某化工厂与相邻的化肥厂联合设计了以下制备 (NH4)2SO4的工艺流程.在如图流程中,沉淀池里物质发生的主要化学反应为:CO2+2NH3+CaSO4(微溶)+ = +(NH4)2SO4.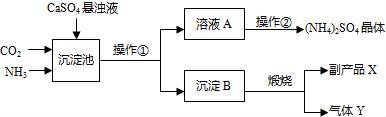

(1)该工艺流程中可循环使用的物质为 (填化学式).进入沉淀池选用CaSO4悬浊液而不用CaSO4溶液的理由是 .沉淀B高温煅烧反应的化学方程式为 .
(2)实验室里操作①称为 ,进行此操作时,用到的玻璃仪器有玻璃棒、 、烧杯.操作②的流程是加热浓缩、 结晶、过滤获得纯净(NH4)2SO4晶体.洗涤所得晶体时不用水,而用饱和(NH4)2SO4溶液的目的是 .
(3)从绿色化学和资源综合利用的角度说明上述流程的主要优点是 .
【分析】根据质量守恒定律分析空格中的物质的化学式;
(1)分析流程图,找出流程中循环利用的物质;根据硫酸钙的溶解性分析用CaSO4悬浊液的原因,分析反应写出反应的方程式;
(2)根据过滤的原理、操作、饱和溶液的特点分析回答.
(3)根据原料的利用、环境的保护分析回答.
【解答】解:由质量守恒定律可知,在反应中有水参加反应,生成物中有碳酸钙生成,所以,方程式是:CO2+2NH3+CaSO4(微溶)+H2O=CaCO3+(NH4)2SO4.
(1)由反应的流程可知,二氧化碳参加反应,在煅烧时又生成了,可循环使用.反应进入沉淀池选用CaSO4悬浊液而不用CaSO4溶液的理由是:CaSO4微溶于水,用悬浊液增加了反应物的量.沉淀B高温煅烧时生成了氧化钙和二氧化碳,反应的化学方程式为:CaCO3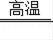
 CaO+CO2↑.
CaO+CO2↑.
(2)操作①是将液体和固体分开,为过滤,进行此操作时,用到的玻璃仪器有玻璃棒、漏斗、烧杯.操作②的流程是加热浓缩、降温结晶、过滤获得纯净(NH4)2SO4晶体.洗涤所得晶体时不用水,而用饱和(NH4)2SO4溶液的目的是:防止晶体被水溶解,提高产量.
(3)从绿色化学和资源综合利用的角度说明上述流程的主要优点是循环利用CO2,提高了原料的利用率等.
故答为:H2O CaCO3(1)CO2,CaSO4微溶于水,用悬浊液增加了反应物的量,CaCO3
 CaO+CO2↑;(2)过滤,漏斗,降温,防止晶体被水溶解,提高产量;(3)循环利用CO2,提高了原料的利用率等.
CaO+CO2↑;(2)过滤,漏斗,降温,防止晶体被水溶解,提高产量;(3)循环利用CO2,提高了原料的利用率等.
【点评】结合流程设计的目的制备硫酸铵,分析流程中所发生的反应,完成对流程的正确认识,此乃解答该问题的方法.


