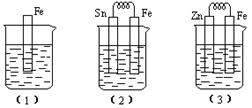
еҰӮдёӢеӣҫжүҖзӨәпјҢзғ§жқҜдёӯйғҪзӣӣжңүзЁҖзЎ«й…ёгҖӮ
пјҲ1пјүдёӯеҸҚеә”зҡ„зҰ»еӯҗж–№зЁӢејҸдёәВ В В В В В В В В В В В В пјҢ
пјҲ2пјүдёӯзҡ„з”өжһҒеҸҚеә”пјҡFeпјҡВ В В В В В В В В В В В В В гҖҒSnпјҡВ В В В В В В В В В В В В В В В В В
SnжһҒйҷ„иҝ‘жә¶ж¶Ізҡ„pHпјҲеЎ«еўһеӨ§гҖҒеҮҸе°ҸжҲ–дёҚеҸҳпјүВ В В В пјҢ
пјҲ3пјүдёӯиў«и…җиҡҖзҡ„йҮ‘еұһжҳҜВ В В В В В В В В В гҖҒе…¶з”өжһҒеҸҚеә”ејҸдёәВ В В В В В В В В В В гҖӮ
жҜ”иҫғпјҲ1пјүгҖҒпјҲ2пјүгҖҒпјҲ3пјүдёӯзәҜй“Ғиў«и…җиҡҖзҡ„йҖҹзҺҮз”ұеҝ«еҲ°ж…ўзҡ„йЎәеәҸжҳҜВ В В В В В В В В В В