(1)第二层离子是____________离子,有____________个,离中心离子的距离为___________。
(2)纳米材料的表面原子占总原子数的比例极大,这是它具有许多特殊性质的根本原因。假设某氯化钠纳米颗粒的大小和形状恰好和NaCl晶胞的相同,求这种纳米颗粒的表面原子占总原子数的百分比。
(3)假设某氯化钠颗粒也是立方体,但其边长为NaCl晶胞边长的10倍,试估算表面原子占总原子数的百分比。
(1)第二层离子是____________离子,有____________个,离中心离子的距离为___________。
(2)纳米材料的表面原子占总原子数的比例极大,这是它具有许多特殊性质的根本原因。假设某氯化钠纳米颗粒的大小和形状恰好和NaCl晶胞的相同,求这种纳米颗粒的表面原子占总原子数的百分比。
(3)假设某氯化钠颗粒也是立方体,但其边长为NaCl晶胞边长的10倍,试估算表面原子占总原子数的百分比。
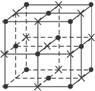
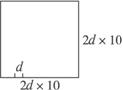
解析:解本题时,要弄清NaCl晶体的排列规则,如图所示,●为Cl-,×为Na+,Na+处于立方体的中心和12条棱的中心,Cl-处于立方体的顶点和面心。离中心Na+最近的是6个处于面心的Cl-(第一层),其次近的是12个Na+(第二层)。将Na+和Cl-均看成小球,它们的间距为d,则在1个NaCl晶胞中共有小球3×3×3=27个,其中只有1个处于体心,另外26个都在表面上,所以表面原子占原子总数的百分比很容易得出。假设将晶胞的立方体边长扩大为原来的10倍,从其表面图可以看出,晶体的边长为20d,可放2×10+1=21个小球,所以共有213=9 261个小球;其中,顶点8个,棱心:21-2=19个,面心:192=361个。所以,表面球为8+19×12+192×6=2 402个。由此得到答案为![]() ×100%=26%。
×100%=26%。
答案:(1)Na+ 12 ![]() d
d
(2)![]() ×100%=96%
×100%=96%
(3)![]() ×100%=26%
×100%=26%