化学是一门以实验为基础的科学,请结合图示回答问题:
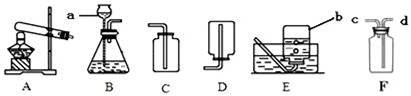

(1)实验室准备用高锰酸钾制取比较纯净的氧气,采用的装置组合是 ,该反应的化学方程式为 ;
(2)实验室用于制取二氧化碳的方程式为 .
采用的常见装置组合为 ,酸液应从 加入(写仪器名称);
若小华想用F装置收集一瓶该气体,则气体由 (填c或d)端进入.
(3)实验室制取二氧化碳一般有以下步骤:
①检查装置的气密性;②按要求连接制取装置;③向长颈漏斗中注入盐酸;④收集气体;⑤向大试管内放入石灰石,操作顺序正确的是
A.①②③④⑤B.②①③④⑤C.②①⑤③④D.③④⑤②①
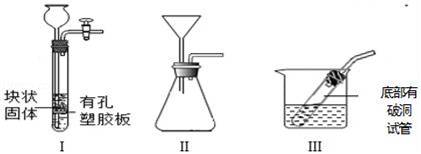
(4)该小组在制取CO2的时候,发现二氧化碳收集好后,反应仍在发生,所以,他们想设计一个能随时控制反应的发生与停止的装置.你觉得下图Ⅰ、Ⅱ、Ⅲ装置中能实现上述意图的是 .

【考点】二氧化碳的实验室制法;氧气的制取装置;氧气的收集方法;制取二氧化碳的操作步骤和注意点;书写化学方程式、.
【分析】(1)根据反应物的状态和反应条件选择发生装置,根据反应原理及方程式书写要求完成化学方程式.
(2)碳酸钙和盐酸常温下反应生成氯化钙、二氧化碳气体和水;根据二氧化碳比空气的密度大,用F装置收集二氧化碳,气体应从长进短出;
(3)本题考查实验室制备并收集二氧化碳的步骤,步骤中注意两个先后:先连接装置,再检查气密性;先加固体,再加液体;
(4)根据实验装置的改进情况来分析.
【解答】解:(1)氧气不易溶于水,密度比空气大,故可用排水法或向上排空气法收集,制取较纯净的氧气,可用排水法;根据反应物是固体,反应条件为加热,所以发生装置选择A;高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气,方程式为2KMnO4
 K2MnO4+MnO2+O2↑;故填:AE;2KMnO4
K2MnO4+MnO2+O2↑;故填:AE;2KMnO4
 K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
(2)碳酸钙和盐酸常温下反应生成氯化钙、二氧化碳气体和水,方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,属于固液常温型,故选择装置B来制取,长颈漏斗是用来添加稀盐酸的;二氧化碳能溶于水,密度比空气大,所以用装置C来收集;二氧化碳比空气的密度大,用F装置收集二氧化碳,气体应从长进短出.故填:CaCO3+2HCl=CaCl2+H2O+CO2↑;BC;长颈漏斗;d;
(3)制取二氧化碳首先是对装置的连接,接着检查装置的气密性,然后是加入药品,即先向反应容器中放人大理石,再向漏斗中注入稀盐酸,最后收集气体;故填:C;
(4)分析图中的装置可以知道,①中的隔板可以放置固体,当用止水夹夹住胶皮管时由于气体不能逸散而使试管中压强增大,将液体压到长颈漏斗中,此时固液分离而使实验停止,若使实验开始只要将止水夹打开即可;装置②中用的普通漏斗,难以实现固液分离,而装置③中破了的试管起到了装置中隔板的作用,具体使用时将试管放入试管中,若停止实验只要将试管取出即可.所以能够实现随时开始或终止实验的装置为:①和③.故填:①和③.




