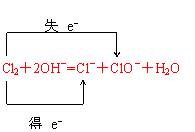(1)已知物质由H、C、Na、O、Cl、Fe元素中的一种或几种组成。请按
(1)已知物质由H、C、Na、O、Cl、Fe元素中的一种或几种组成。请按要求回答。
①酸性氧化物的化学式 。(写一种,下同)
②有机物的化学式 。
③碱性氧化物与酸反应的离子方程式 。
(2)依据题意填空。
①填入合适的符号。 + 2H+ = CO2↑+ H2O + Ba2+
②写出离子方程式为Cu2+ + 2OH- =Cu(OH)2↓ 的化学方程式。 (写一个)
③用氯化铁溶液腐蚀铜线路板的离子方程式为________________。
④将氯气通入NaOH 溶液中可生产消毒液。写出发生反应的离子方程式______,并用单线桥或双线桥标出电子转移的方向和数目。____________________________
(3)选择合适的试剂除去下列括号内的杂质。
| | 选择的试剂 | 操作 | 选择的试剂 |
| ①Cu(Fe) | | ②CO2气体(HCl) | |
【答案】(1)①CO2;②CH4;③ Na2O+2H+=2Na++H2O;(2)①BaCO3;②CuSO4+2NaOH= Cu(OH)2↓+Na2SO4;③2Fe3++Cu = 2Fe2++Cu2+;④Cl2+2OH-=Cl-+ClO-+H2O,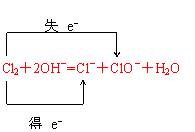
 ;(3)①稀盐酸或稀硫酸或磁铁;②饱和碳酸氢钠。
;(3)①稀盐酸或稀硫酸或磁铁;②饱和碳酸氢钠。
【解析】
试题分析:(1)①酸性氧化物是与水反应只生成酸(化合价不变),或与碱反应生成盐和水(化合价不变),因此酸性氧化物是CO2、Cl2O7、Cl2O2、Cl2O3等;②有机物是含碳的化合物,但CO2、CO、碳酸盐、氰化物等不属于有机物,因此属于有机物是CH4、CH3Cl、CH3CH2OH等;③碱性氧化物都是金属氧化物,如Na2O、Fe2O3等,Na2O+2H+=2Na++H2O,Fe2O3+6H+=2Fe3++3H2O;(2)①反应前后原子和元素守恒,离子反应方程式电荷守恒,因此空白处填写BaCO3;②可溶性铜盐和可溶性强碱,没有其他反应,因此应是CuSO4+2NaOH=Cu(OH)2↓+H2SO4等;③铜和Fe3+反应,其离子反应方程式为:Cu+2Fe3+=2Fe2++Cu;④氯气和NaOH发生歧化反应,离子反应是Cl2+2OH-=Cl-+ClO-+H2O,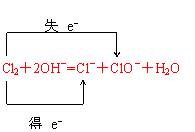
 ;(3)根据金属活动顺序表,应用稀硫酸或盐酸;盐酸的酸性强于碳酸,应用饱和碳酸氢钠溶液,但不能用饱和碳酸钠溶液,因为Na2CO3+CO2+H2O=2NaHCO3。
;(3)根据金属活动顺序表,应用稀硫酸或盐酸;盐酸的酸性强于碳酸,应用饱和碳酸氢钠溶液,但不能用饱和碳酸钠溶液,因为Na2CO3+CO2+H2O=2NaHCO3。
考点:考查物质分类、离子反应方程式的书写、物质除杂等知识。