卤素单质及其化合物在生产和生活中有广泛应用。
Ⅰ、氟化钠主要用作农作物杀菌剂、杀虫剂、木材防腐剂。实验室以氟硅酸(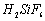 )等物质为原料、通过下图所示的流程制取较纯净的氟化钠,并得到副产品氯化铵:
)等物质为原料、通过下图所示的流程制取较纯净的氟化钠,并得到副产品氯化铵:

已知:20℃时氯化铵的溶解度为37.2 g,氟化钠的溶解度为4 g,Na2SiF6微溶于水。
请回答下列有关问题:
(1)完成并配平上述流程中①、②的化学反应方程式:
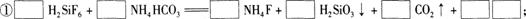
② 。
(2)操作Ⅲ分为两步,其顺序是 (填写所选序号)。
a、过滤 b、加热浓缩 c、冷却结晶 d、洗涤
操作Ⅱ是洗涤、干燥,其目的是 ,在操作Ⅰ~V中与之相同的操作步骤是 。
(3)流程①中NH4HCO3必须过量,其原因是 。
Ⅱ、紫菜与海带类似,是一种富含生物碘的海洋植物,可用于食用补碘。以下为某兴趣小组模拟从紫菜中提取碘的过程:
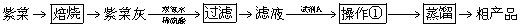
已知:商品紫菜轻薄松脆,比海带更易被焙烧成灰(此时碘转化为碘化物无机盐)。
(4)将焙烧所得的紫菜灰与足量的双氧水和稀硫酸作用,写出反应的离子方程式:
。
(5)操作①中涉及两步操作,名称是 ,所用的主要玻璃仪器为 ,所用试剂A最好选用表格中的 (填试剂名称)。
| | 乙醇 | 四氯化碳 | 裂化汽油 | 碘(晶体) |
| 密度/g、cm-3 | 0.7893 | 1.595 | 0.71~0.76 | 4.94 |
| 沸点/℃ | 78.5 | 76.8 | 25~232 | 184.35 |
(6)将下列装置图中缺少的必要仪器补画出来,以最终将单质碘与试剂A分离:

【知识点】制备实验方案设计、物质除杂、反应方程式书写
【答案解析】(1)H2SiFe+6NH4HCO3 ===6NH4F+H2SiO3↓+6CO2↑+3H2O(1分)
NH4F+NaCl ===NaF↓+NH4Cl(1分)
(2)bc(1分) 除去氟化钠表面的氯化铵等可溶性杂质(1分) V(1分)
(3)使氟硅酸完全反应,避免析出Na2SiFe而混入杂质(1分)
(4)H2O2+2I-+2H+ I2+2H2O(2分)
(5)萃取、分液;分液漏斗;四氯化碳
 (6)
(6)
(温度计、石棉网、锥形瓶各1分,共3分)
解析:(1)根据工艺流程图知,反应物是氟硅酸、碳酸氢铵和水,生成物是二氧化碳和硅酸,根据元素守恒知,生成物中含有氟化铵,所以方程式为H2SiFe+6NH4HCO3 ===6NH4F+H2SiO3↓+6CO2↑+3H2O; 根据物质在水中的溶解度知,20℃时氟化铵的溶解度远远大于氟化钠,所以在滤液中加入NaCl的目的是:增加Na+浓度,促进氟化铵转化为NaF沉淀,从而得到氟化钠,反应的化学方程式为:NH4F+NaCl═NaF↓+NH4Cl;
从溶液中获取固体的方法是:蒸发浓缩,析出大量固体后冷却结晶;操作Ⅱ是洗涤、干燥,其目的是除去氟化钠表面的氯化铵等可溶性杂质;操作V也是相同步骤;
反应过程中,一方面碳酸氢铵过量能促使氟硅酸全部反应,另一方面防止在进行反应Ⅱ时有残余H2SiF6与NaCl反应,生成Na2SiF6沉淀,使所得产品不纯;
双氧水具有强氧化性,酸性条件下,双氧水氧化碘离子生成碘单质,自身被还原生成水,反应方程式为H2O2+2I-+2H+=I2+2H2O;
通过过滤,得到不溶的残渣,滤液为碘单质溶液,利用有机溶剂萃取出碘单质,萃取剂的选取标准是:溶质在萃取剂中的溶解度大于在原溶剂中的溶解度,溶质和萃取剂不反应,萃取剂和原来溶剂不能互溶,题干中提供的四中物质,乙醇和水能互溶,不能做萃取剂,裂化汽油含有不饱和碳碳双键能与碘发生加成反应,不能做萃取剂,四氯化碳符合萃取剂的选取标准,所以可以用四氯化碳作萃取剂;
【思路点拨】本题考查了实验方案设计中的有关问题,难度不大,能准确获取题目中有用的信息进行利用是解本题的关键。
![]() )等物质为原料、通过下图所示的流程制取较纯净的氟化钠,并得到副产品氯化铵:
)等物质为原料、通过下图所示的流程制取较纯净的氟化钠,并得到副产品氯化铵: 
![]()
![]()


