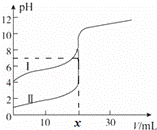
室温下,用0.1mol/L氨水分别滴定20.0mL、0.1mol/L的盐酸和醋酸,曲线如图所示,下列说法正确的( )
|
| A. | I曲线表示的是滴定盐酸的曲线 |
|
| B. | x=20 |
|
| C. | 滴定过程中 |
|
| D. | 当I曲线和II曲线pH均为7时,一溶液中的c(Cl﹣)等于另一溶液中的c(CH3COO﹣) |
室温下,用0.1mol/L氨水分别滴定20.0mL、0.1mol/L的盐酸和醋酸,曲线如图所示,下列说法正确的( )

|
| A. | I曲线表示的是滴定盐酸的曲线 |
|
| B. | x=20 |
|
| C. | 滴定过程中 |
|
| D. | 当I曲线和II曲线pH均为7时,一溶液中的c(Cl﹣)等于另一溶液中的c(CH3COO﹣) |
考点:
中和滴定..
专题:
电离平衡与溶液的pH专题.
分析:
A.0.1mol/L的盐酸的pH=1,结合滴定曲线开始时的pH来判断;
B.根据两者恰好反应生成氯化铵,氯化铵水解溶液呈酸性,要使溶液呈中性,则氨水应过量;
C.根据氨水的电离平衡常数只与温度有关以及c(OH﹣)在增大;
D.根据当I曲线和II曲线pH均为7时,在盐酸中,氨水过量,在醋酸中,氨水恰好反应,根据溶液中电荷守恒来解答.
解答:
解:A.滴定开始时0.1mol/L盐酸pH=1,0.1mol/L醋酸pH>1,所以滴定盐酸的曲线是图Ⅱ,滴定醋酸的曲线是图Ⅰ,故A错误;
B.用0.1mol/L氨水滴定20.0mL、0.1mol/L的盐酸,两者恰好反应,消耗20.0mL、0.1mol/L氨水,但反应生成氯化铵,氯化铵水解溶液呈酸性,所以溶液呈中性,碱应过量,故B错误;
C.NH3•H2O的电离常数Kb=![]() 只与温度有关,随着氨水的加入,C(OH﹣)在增大,所以中
只与温度有关,随着氨水的加入,C(OH﹣)在增大,所以中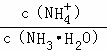 的值逐渐减小,故C正确;
的值逐渐减小,故C正确;
D.当I曲线和II曲线pH均为7时,分别存在电离平衡:c(NH4+)+c(H+)=c(Cl﹣)+c(OH﹣);c(NH4+)+c(H+)=c(CH3COO﹣)+c(OH﹣),都存在:c(H+)=c(OH﹣),所以c(NH4+)=c(Cl﹣),c(NH4+)=c(CH3COO﹣),在盐酸中,氨水过量,在醋酸中,氨水恰好反应,所以盐酸中c(NH4+)大,则c(Cl﹣)>c(CH3COO﹣),故D错误;
故选C.
点评:
本题考查酸碱混合溶液酸碱性判断及溶液中离子浓度大小比较,涉及盐类的水解、电离常数等知识,注意醋酸铵溶液呈中性,题目难度中等