部分弱酸的电离平衡常数如下表:下列说法正确的是( )
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数 | K=1.77×10﹣4 | K=4.9×10﹣10 | K1=4.2×10﹣7 K2=5.6×10﹣11 |
A.0.1mol•L﹣1NaHCO3溶液中浓度的大小:c(Na+)>c(HCO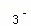 )>c(H+)>c(OH﹣)
)>c(H+)>c(OH﹣)
B.少量的CO2通入到NaCN溶液中 CN﹣+H2O+CO2=HCN+HCO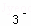
C.用0.1mol•L﹣1NaOH溶液中和等浓度的HCN和HCOOH时前者所需NaOH溶液体积大
D.0.1mol•L﹣1HCOONa溶液比0.1mol•L﹣1NaCN溶液所含离子总数小
【考点】弱电解质在水溶液中的电离平衡.
【分析】A、碳酸氢钠中碳酸氢根离子水解程度大于电离程度而使其溶液呈碱性;
B、碳酸的酸性比HCN强,少量二氧化碳通入NaCN溶液中,生成碳酸氢根;
C、中和碱的能力与酸性强弱无关;
D、没有指明溶液体积,无法比较离子数目多少.
【解答】解:A、碳酸氢钠中碳酸氢根离子水解程度大于电离程度而使其溶液呈碱性,所以c(H+)<c(OH﹣),故A错误;
B、碳酸的酸性比HCN强,少量二氧化碳通入NaCN溶液中,生成碳酸氢根,其离子方程式为:CN﹣+H2O+CO2=HCN+HCO3﹣,故B正确;
C、相同物质的量的HCN和HCOOH,中和碱的能力相同,元数相同的酸中,酸中和碱的能力与酸的物质的量成正比,与酸的强弱无关,所以用0.1mol•L﹣1 NaOH溶液中和等浓度的HCN和HCOOH时,二者需要NaOH溶液体积相等,故C错误;
D、没有指明溶液体积,无法比较离子数目多少,故D错误;
故选B.
【点评】本题考查了弱电解质的电离及盐类水解,明确弱酸的电离平衡常数与酸性强弱、酸根离子水解程度之间的关系即可解答,易错选项是C,题目难度不大.
![]() )>c(H+)>c(OH﹣)
)>c(H+)>c(OH﹣)![]()
