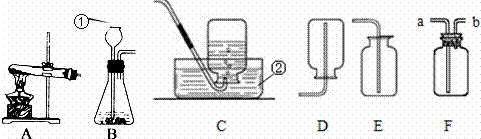
(1)写出标号仪器的名称:① ;② .
(2)实验室用高锰酸钾制取氧气,反应的符号表达式为 ,应选用的发生装置是 (填字母,下同),以高锰酸钾为试剂利用此装置制取氧气时,还要做的改进是 ,其作用是 .
用E装置收集氧气的依据是 ,检验氧气是否集满的方法是 .用F装置收集氧气时,气体应从 (填“a”或“b”)管通入.
(3)某同学想用过氧化氢溶液和二氧化锰混合制取较纯净的氧气,他应选用的装置组合是 .由于该同学动作太慢,氧气还没有收集满,容器内的反应就停止了,若想集满这瓶气体,在不拆卸装置的前提下,请你帮他想两种方法:
① ;
② .
(4)通过查阅资料得知:氨气(NH3)是一种密度比空气小且极易溶于水的气体,其水溶液称为氨水.实验室用加热氯化铵和氢氧化钙的固体混合物的方法来制取氨气,你认为应选择的发生装置是 ,收集装置是 .
1909年化学家哈伯在实验室首次合成了氨.2007年化学家格哈德•埃特尔在哈伯研究所证实了氢气与氮气在固体催化剂表面合成氨的过程,获得诺贝尔化学奖.将氢气和氮气在高温、高压和催化剂的条件下合成氨(NH3).反应的化学方程式为:高温、高压 催化剂N2+3H2═2NH3用 、
、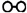 、
、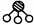 分别表示N2、H2、NH3.观察图,写出符合在催化剂表面
分别表示N2、H2、NH3.观察图,写出符合在催化剂表面
合成氨反应过程的顺序: (将下面五张图按反应过程顺序用序号排列).

考点:
氧气的制取装置;氧气的收集方法;氧气的检验和验满;制取氧气的操作步骤和注意点;微粒观点及模型图的应用;化学反应的实质;书写化学方程式、文字表达式、电离方程式.. | | 专题: | 常见气体的实验室制法、检验、干燥与净化. |
| 分析: | (1)要掌握各种仪器的名称; (2)高锰酸钾受热能分解生成锰酸钾、二氧化锰和氧气,据反应物的状态和反应的条件选择发生装置,据氧气能够使得带火星的木条复燃的性质进行验满,氧气不易溶于水,密度比空气大; (3)用过氧化氢溶液制取氧气不需要加热,可以用二氧化锰作催化剂;据催化剂在化学反应前后其质量和化学性质不变分析; (4)据药品的状态和反应的条件选择发生装置,据气体的密度和溶解性选择收集装置;化学变化的实质为:反应物的分子在一定条件下被破坏,分解成原子,然后这些原子重新组合成新的分子. |
| 解答: | 解(1)由图可知:①是长颈漏斗;②是水槽. (2)加热高锰酸钾会产生锰酸钾、二氧化锰和氧气,反应的符号表达式为 2KMnO4 K2MnO4+MnO2+O2↑反应物是固体,反应条件是加热,故应选用的发生装置是A,以高锰酸钾为试剂利用此装置制取氧气时,还要做的改进是在试管口塞一团棉花,其作用是防止高锰酸钾粉末进入导管.用E装置收集氧气的依据是氧气密度比空气大,检验氧气是否集满的方法是将带火星木条放在瓶口,若木条复燃,表示满了.用F装置收集氧气时,由于氧气的密度大于空气,故气体应从a管通入. K2MnO4+MnO2+O2↑反应物是固体,反应条件是加热,故应选用的发生装置是A,以高锰酸钾为试剂利用此装置制取氧气时,还要做的改进是在试管口塞一团棉花,其作用是防止高锰酸钾粉末进入导管.用E装置收集氧气的依据是氧气密度比空气大,检验氧气是否集满的方法是将带火星木条放在瓶口,若木条复燃,表示满了.用F装置收集氧气时,由于氧气的密度大于空气,故气体应从a管通入. (3)某同学想用过氧化氢溶液和二氧化锰混合制取较纯净的氧气,应该用排水法收集氧气气体较纯净,故他应选用的装置组合是BC.想集满瓶中氧气可以采取的方法是①由于二氧化锰是催化剂,化学反应前后其质量和化学性质不变,故再加入适量的双氧水会使反应继续进行; ②从分液漏斗向锥形瓶内加水,将锥形瓶内的氧气压入集气瓶中. (4)实验室用加热氯化铵和氢氧化钙的固体混合物的方法来制取氨气,装置类型“属于固体加热型”,应选择的发生装置是 A;据氨气(NH3)是一种密度比空气小且极易溶于水的气体,故只能采用向下排空气法收集,故收集装置是 D或F. 分析题中五个图是准确解答本题的核心. 图①所示为附在催化剂表面的原子,此图应该是变化中分解成原子的一个过程; 图②中形成了氨气分子,应为原子重新组合成新分子的过程; 图③表示出新分子与催化剂分离,应为变化过程的最后环节; 图④中分子仍然为原反应物的分子,和图⑤相比较,可判断是反应物与催化剂相结合的一个过程; 图⑤中的分子仍为氮气分子和氢气分子,且反应物分子还没接触到催化剂,此图应表示反应最初的过程. 故填:⑤④①②③ 故答案为:(1)长颈漏斗 水槽 (2)2KMnO4 K2MnO4+MnO2+O2↑ A 在试管口塞一团棉花 防止高锰酸钾粉末进入导管 K2MnO4+MnO2+O2↑ A 在试管口塞一团棉花 防止高锰酸钾粉末进入导管 氧气密度比空气大 将带火星木条放在瓶口,复燃,满了 a (3)BC ①再加入适量的双氧水使反应继续进行 ②从分液漏斗向锥形瓶内加水,将锥形瓶内的氧气压入集气瓶中 (4)A D或F:⑤④①②③ |
| 点评: | 本题主要考查实验室制取氧气的方法和化学方程式的书写等方面的知识,书写化学方程式时要注意遵循质量守恒定律. |

![]() 、
、![]() 、
、![]() 分别表示N2、H2、NH3.观察图,写出符合在催化剂表面
分别表示N2、H2、NH3.观察图,写出符合在催化剂表面
