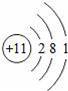
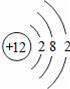
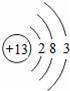
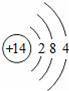
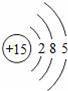
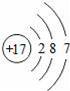
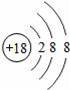
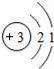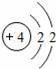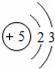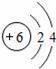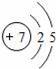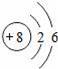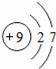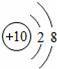“化学家的主要工作是耕耘元素周期表”.如图所示为元素周期表中部分元素的相关信息.请利用图示信息回答相关问题:
(1)锂原子的核电荷数为 .
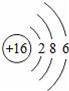
(2)16号元素的原子在化学反应中比较容易 (选填“得”或“失”)电子.该元素属于 (选填“金属”或“非金属”)元素.
(3)写出表中关于8号元素的一条信息: .
(4)在金属活动性顺序表中镁的活动性比铝的活动性强,试从原子结构的角度说明其原因: .
【考点】元素周期表的特点及其应用.
【专题】压轴实验题;化学用语和质量守恒定律.
【分析】(1)根据元素周期表可知锂原子的原子序数,原子序数=核电荷数;
(2)根据元素周期表分析16号元素的原子结构示意图,由最外层电子数判定其得失电子的情况;由其名称分析其元素类别;
(3)8号元素的原子最外层电子数是6,在化学反应中其原子比较容易得到2个电子变成离子;
(4)镁原子的最外层电子数是2,铝原子的最外层电子数是3,在化学反应中镁原子更易失去电子.
【解答】解:(1)根据元素周期表可知锂原子的原子序数为3,由原子序数=核电荷数,因此锂原子的核电荷数为3;
故答案为:3;
(2)16号元素原子结构示意图是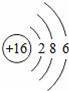
 ,最外层电子数是6,在化学反应中其原子比较容易得到2个电子变成离子;16号元素是硫,属于非金属元素;
,最外层电子数是6,在化学反应中其原子比较容易得到2个电子变成离子;16号元素是硫,属于非金属元素;
故答案为:得;非金属;
(3)8号元素的原子最外层电子数是6,在化学反应中其原子比较容易得到2个电子变成离子;
故答案为:化学反应中其原子比较容易得到电子;
(4)从表可以看出,镁铝的电子层数相同,镁原子的最外层电子数是2,铝原子的最外层电子数是3,在化学反应中镁原子更易失去电子,因此在金属活动性顺序表中镁的活动性比铝的活动性强.
故答案为:镁铝的电子层数相同,镁原子的最外层电子数是2,铝原子的最外层电子数是3,在化学反应中镁原子更易失去电子.
【点评】本题考查学生根据原子结构示意图分析总结元素周期律及对元素的性质与最外层电子数的关系的理解与掌握,并能在解题中灵活应用.