在宏观、微观和符号之间建立联系是化学学科的重要思维方式
(1)根据如图1粒子结构示意图,回答问题:
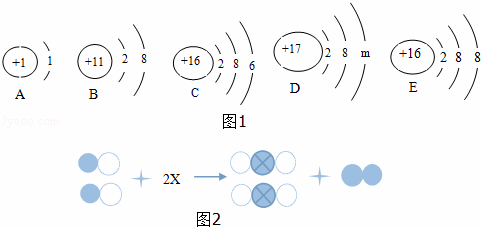
①上述示意图图1中,共包含 种元素,它们之间的本质区别是 不同
②A、B、C、E中属于阴离子的是 (填离子符号)
③若D表示某元素的原子,则m= ,该粒子在化学变化中容易 (选填“得到”或“失去”)电子④若D为离子,则BD组成的化合物的化学式为
(2)图2表示某反应的微观示意图,其中不同的球代表不同元素的原子,请画出X分子的微观示意图
在宏观、微观和符号之间建立联系是化学学科的重要思维方式
(1)根据如图1粒子结构示意图,回答问题:

①上述示意图图1中,共包含 种元素,它们之间的本质区别是 不同
②A、B、C、E中属于阴离子的是 (填离子符号)
③若D表示某元素的原子,则m= ,该粒子在化学变化中容易 (选填“得到”或“失去”)电子④若D为离子,则BD组成的化合物的化学式为
(2)图2表示某反应的微观示意图,其中不同的球代表不同元素的原子,请画出X分子的微观示意图
考点: 原子结构示意图与离子结构示意图;微粒观点及模型图的应用
专题: 化学反应模拟图型;化学用语和质量守恒定律
分析: (1)①根据元素的定义分析回答;
②根据原子结构中,原子序数=核电荷数=核外电子数;对于阴离子,核内质子数<核外电子数;阳离子,核内质子数>核外电子数进行解答;
③根据元素的性质与原子的最外层电子数的关系分析回答;
(2)根据质量守恒定律反应前后原子的种类及数目不变分析回答
解答: 解:(1)①质子数决定元素的种类,上述示意图图1中,共有4种质子数,共包含四种元素,它们之间的本质区别是质子数不同
②在E中,核内质子数=16<核外电子数=18,属于阴离子,是硫离子,符号为:S2﹣
③若D表示某元素的原子,由于在原子中核内质子数=核外电子数,则m=17﹣2﹣8=7,最外层电子数大于4,该粒子在化学变化中容易得到电子④由结构示意图可知,若D为离子,应为氯离子,化合价为﹣1价,B为钠离子,化合价为+1价,则BD组成的化合物的化学式为NaCl
(2)图2表示某反应的微观示意图,其中不同的球代表不同元素的原子,由质量守恒定律反应前后原子的种类及数目不变可知,X分子的微观示意图为:![]()
故答为:(1)①四质子数;②S2﹣;③7,NaCl;(2)![]()
点评: 本题较全面地考查学生对微粒结构示意图的掌握情况,要求学生会根据结构示意图的特点判断元素的种类,元素的性质等