将一定质量的镁铝合金投入100 mL一定浓度的盐酸中,合金完全溶解。向所得溶液中滴加浓度为5 mol/L的NaOH溶液,生成的沉淀跟加入的NaOH溶液的体积关系如图。(横坐标体积单位是mL,纵坐标质量单位是g)求:
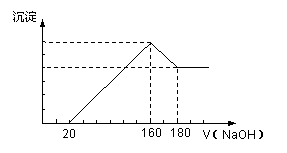

(1)加入NaOH溶液0--20mL过程中反应方程式为:_______________________。160--180mL过程中反应方程式为_______________________。
(2)合金中Mg的质量为____________g。所用HCl的物质的量浓度为____________mol/L。
【答案】(1)HCl + NaOH══NaCl+ H2O ;Al(OH)3 + NaOH ══NaAlO2 +2 H2O
(2)4.8 ; 8
【解析】
试题分析:(1)加入NaOH溶液0--20mL过程中溶液无沉淀产生,显然盐酸过量,发生氢氧化钠与盐酸中和反应:HCl + NaOH══NaCl+ H2O,
160--180mL过程中沉淀质量减少,发生氢氧化铝与氢氧化钠发生,沉淀溶解:
Al(OH)3 + NaOH ══NaAlO2 +2 H2O
(2)Mg(OH)2质量就是11.6g,(因Al(OH)3溶于过量的NaOH生成NaAlO2.)
所以Mg~Mg(OH)2~2HCl
24 58 2
m(Mg) 11.6 n(HCl)
解出来是m(Mg)=4.8g
HCl是0.4mol
(2)与合金反应后HCl有剩余
消耗了0.025=0.1mol的NaOH.所以HCl有0.1mol
3HCl~Al~Al(OH)3
3 1 78
n(HCl) 7.8
算出n(HCl)=0.3mol
一共就是0.4mol +0.1mol +0.3mol =0.8molHCl
所以c(HCl)=0.8/0.1=8mol/L
考点:化学方程式计算,镁铝的化学性质。
点评:本题考查混合物的计算,注意判断加入的NaOH溶液反应的过程,分析各过程的产物为解答该题的关键,同时考查了图象的分析应用


