如图是实验室制取氧气的装置.
(1)实验中,若产生氧气的速率太大,不利于收集.为了减小反应速率,可以进行的合理操作是 ,该反应的化学方程式是 .
(2)若需要一瓶干燥的氧气,应该将装置A产生的氧气通过干燥装置后再与 (填“B”、“C”或“D”)相连.
(3)若用排水法收集了一瓶气体,并用带火星的木条检验,发现木条没有复燃,可能的原因有
A.实验所用的过氧化氢溶液的浓度太低
B.开始收集时,倒置于水槽中的集气瓶未装满水
C.导管口一出现气泡就立即收集.
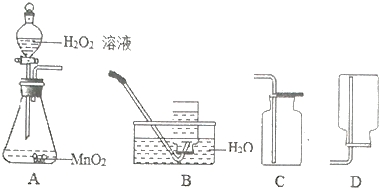
如图是实验室制取氧气的装置.
(1)实验中,若产生氧气的速率太大,不利于收集.为了减小反应速率,可以进行的合理操作是 ,该反应的化学方程式是 .
(2)若需要一瓶干燥的氧气,应该将装置A产生的氧气通过干燥装置后再与 (填“B”、“C”或“D”)相连.
(3)若用排水法收集了一瓶气体,并用带火星的木条检验,发现木条没有复燃,可能的原因有
A.实验所用的过氧化氢溶液的浓度太低
B.开始收集时,倒置于水槽中的集气瓶未装满水
C.导管口一出现气泡就立即收集.

【考点】氧气的制取装置;氧气的收集方法;书写化学方程式、文字表达式、电离方程式.
【专题】实验操作型;氧气、氢气的性质与用途;常见仪器及化学实验基本操作;常见气体的实验室制法、检验、干燥与净化.
【分析】(1)根据过氧化氢溶液和二氧化锰接触就反应,要想减小反应速率,就要让二者少接触,由于二氧化锰加入量是一定的,只能改变过氧化氢溶液的加入量,过氧化氢在二氧化锰的催化作用下生成水和氧气进行分析;
(2)根据氧气既可用排水法收集,又可用向上排空气法收集;但排水法会使收集的氧气中含有水分,所以收![]() 集干燥的气体只能用向上排空气法进行分析;
集干燥的气体只能用向上排空气法进行分析;
(3)从“用带火星的木条检验,发现木条没有复燃”说明集气瓶内没有氧气或者氧气的浓度很小去分析解答.
【解答】解:(1)为了减小反应速率,可以调节分液漏斗活塞,过氧化氢在二氧化锰的催化作用下生成水和氧气,化学方程式为:2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(2)氧气既可用排水法收集,又可用向上排空气法收集;但排水法会使收集的氧气中含有水分,故收集干燥的气体只能用向上排空气法,故选:C;
(3)“用带火星的木条检验,发现木条没有复燃”说明集气瓶内没有氧气或者氧气的浓度很小;
A、实验所用的过氧化氢溶液的溶质质量分数太小,反应速率会变慢,但产生的氧气会很纯,故A错误;
B、倒置于水槽中的集气瓶未装满水,说明集气瓶中原来有空气,可能使氧气的量太少,故B正确;
C、收集氧气时,刚开始冒出的是空气,也会导致集气瓶内氧气的浓度很小,故C正确.
故选:BC.
故答案为:(1)调节分液漏斗活塞,2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(2)C;
(3)BC.
【点评】本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.