某课外活动小组设计了以下实验验证Ag与浓硝酸反应的过程中可能产生NO。其实验流程图如下:

(1)测定硝酸的物质的量反应结束后,从如图装置B中所得100 mL溶液中取出25.00 mL溶液,用0.1 mol·L-1的NaOH溶液滴定,用酚酞作指示剂,滴定前后的滴定管中液面的位置如上图所示。在B容器中生成硝酸的物质的量为______ mol,则Ag与浓硝酸反应过程中生成的NO2在标准状况下的体积为___________mL。
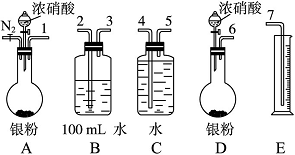
(2)测定NO的体积
①从如图所示的装置中,你认为应选用________装置进行Ag与浓硝酸反应实验,选用的理由是_______。
②选用如图所示仪器组合一套可用来测定生成NO体积的装置,其合理的连接顺序是__________(填各导管口编号)。
③在测定NO的体积时,若量筒中水的液面比集气瓶的液面要低,此时应将量筒的位置_______(填“下降”或“升高”),以保证量筒中的液面与集气瓶中的液面持平。
(3)气体成分分析
若实验测得NO的体积为112.0 mL(已折算到标准状况),则Ag与浓硝酸反应的过程中______(填“有”或“没有”)NO产生,作此判断的依据是_________。
【答案】(16分) (每空2分)(1)0.008 268.8
(2)①A 因为A装置可以通N2将装置中的空气排尽,防止NO被空气中的O2氧化 ②123547 ③升高
(3)有 因为NO2与水反应生成的NO的体积小于收集到的NO的体积(89.6<112.0)
【解析】
试题分析:(1)B容器中是二氧化氮和水反应生成硝酸和一氧化氮;100mL溶液中取出25.00mL溶液,用0.1mol/L的NaOH溶液滴定,用酚酞做指示剂,终点时,消耗氢氧化钠溶液的体积为20.4ml-0.4ml=20.00ml;所以生成硝酸25.00mL溶液中含有0.02L×0.1mol/L=0.002mol;则B容器中生成硝酸的物质的量为0.008mol;由3NO2+H2O=2HNO3+NO可知金属与硝酸反应生成二氧化氮物质的量为0.012mol,其体积为0.012×22.4=268.8L。故答案为:0.008mol;0.012mol;
(2)①一氧化氮气体易被氧化生成二氧化氮对验证产生干扰,AD相比A装置利用氮气可以把装置中的空气排净;故答案为:A;因为A装置可以通入N2将装置中的空气排尽,防止NO被空气中O2氧化。
②用A进行银和浓硝酸的反应,用水吸收生成的二氧化氮气体,导气管长进短出,可以用排水量气法测定一氧化氮气体的体积,排水集气瓶导气管应短进长出,连接顺序为:123547,故答案为123547;
③读数之前应保持内外压强相同,恢复到室温下读取量筒中液体的体积,故答案为:等液体冷却到室温,并使集气瓶和量筒内液面相平;
(3)实验测得NO的体积为112.0mL(已这算到标准状况),依据上述计算得到银和浓硝酸生成二氧化氮气体物质的量为0.012mol,依据3NO2+H2O=2HNO3+NO;计算得到一氧化氮气体物质的量为0.004mol,标准状况下体味为0.004×2.4L/mol=0.0896L=89.6mL<112.0mL可知银和硝酸反应生成一氧化氮气体,故答案为:有;因为NO2与水反应生成的NO的体积小于收集到的NO的体积89.6<112.0
考点: 性质实验方案的设计


