老师从实验桌上拿出两瓶常用的但标签已经模糊不清的试剂,分别是固体和液体,他取少量试剂在试管中混合,立即产生一种无色气体.我们对此气体展开了系列探究:
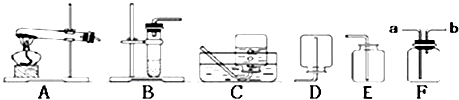
(1)猜想:我认为产生的气体能使带火星的木条复燃,我能写出此反应的化学方程式: ,我知道它的反应类型是 .我想制取比较纯净的该气体,发生装置将选取图中的 (填序号,以下同),收集装置选取 .如果用图中的F装置收集该气体,气体应从 端(填“a”或“b”)导入;用F装置收集该气体验满的方法是 .
(2)我猜想无色气体还可能是另外一种密度比空气大的气体.实验室制取该气体的反应的化学方程式为: .请写出实验室检验该气体的化学反应的化学方程式 .
【考点】常用气体的发生装置和收集装置与选取方法;实验室制取氧气的反应原理;氧气的检验和验满;二氧化碳的实验室制法;反应类型的判定;书写化学方程式、文字表达式、电离方程式.
【专题】实验方法和过程的探究;常见气体的实验室制法、检验、干燥与净化.
【分析】(1)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
氧气的密度比空气的密度大,不易溶于水,能够支持燃烧,能使带火星的木条复燃;
(2)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳;
二氧化碳能使澄清石灰水变浑浊,因此可以用澄清石灰水检验二氧化碳.
【解答】解:(1)猜想:产生的气体能使带火星的木条复燃,能使带火星的木条复燃的气体是氧气,过氧化氢在二氧化锰的催化作用下分解生成水和氧气,反应的化学方程式为:
2H2O2 2H2O+O2↑,属于分解反应;
2H2O+O2↑,属于分解反应;
利用过氧化氢制取氧气不需要加热,应该用B装置作为发生装置;
因为氧气的密度比空气大,可以用向上排空气法收集,即用E装置收集,氧气不易溶于水,可以用排水法收集,即用C装置收集,用排水法收集的氧气比用排空气法收集的氧气纯净;
如果用图中的F装置收集该气体,由于氧气密度比空气大,气体应从a端导入;
用F装置收集该气体验满的方法是:将带火星的木条放在b导管口,若木条复燃,证明氧气已收集满.
故填:2H2O2 2H2O+O2↑;分解反应;B;C;a;将带火星的木条放在b导管口,若木条复燃,证明氧气已收集满.
2H2O+O2↑;分解反应;B;C;a;将带火星的木条放在b导管口,若木条复燃,证明氧气已收集满.
(2)猜想无色气体还可能是另外一种密度比空气大的气体,该气体是二氧化碳,实验室制取该气体的反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
可以用澄清石灰水检验二氧化碳,二氧化碳能使澄清的石灰水变浑浊,是因为二氧化碳和石灰水中的氢氧化钙反应生成了碳酸钙沉淀和水,反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O.
故填:CaCO3+2HCl=CaCl2+H2O+CO2↑;Ca(OH)2+CO2═CaCO3↓+H2O.
【点评】合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

