某研究小组为了探究一种无机矿物盐x(仅含四种元素)的组成和性质.设
计并完成了如下实验:
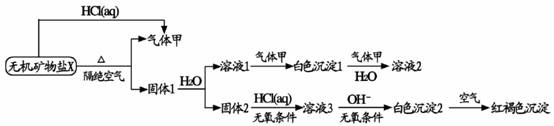
另取10.80gX在惰性气流中加热至完全分解,得到6.40g固体1。请回答下列问题:
(1)X的化学式为 ,在隋性气流中加热X至完全分解的化学反应方程式为
。
(2)一定条件下,气体甲与固体1中的某种成分可能发生氧化还原反应,写出一个可能的化学反应方程式 。并设计实验方案验证该反应的产物 。
(3)白色沉淀1中金属元素的原子结构示意图为 ,气体甲的电子式为 。
(4)自色沉淀2在空气中变成红褐色沉淀的原因是 。
(用化学反应方程式表示)
【知识点】无极推断题C3 D3 D5
【答案解析】(1) CaFe(CO3)2 CaFe(CO3)2  CaO+FeO+2CO2↑
CaO+FeO+2CO2↑
(2)2FeO+CO2 Fe2O3+CO 检验方法:将固体用盐酸溶解,加入KSCN溶液,若溶液呈红色,证明有Fe(III);检测CO:将气体通入灼烧CuO,黑色固体变成红色。
Fe2O3+CO 检验方法:将固体用盐酸溶解,加入KSCN溶液,若溶液呈红色,证明有Fe(III);检测CO:将气体通入灼烧CuO,黑色固体变成红色。
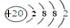
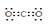
(4)4Fe(OH)2+O2+2H2O=4Fe(OH)3
解析:气体甲能与溶液1先产生沉淀后沉淀溶解,则是二氧化碳与氢氧化钙的反应,说明固体X含有钙元素,隔绝空气加热产生气体二氧化碳,说明X含有碳、氧元素。同时根据溶液3先产生白色沉淀后产生红褐色,可得出固体1还含有铁元素
(1)X的化学式为:CaFe(CO3)2 在惰性气流中加热至完全分解的化学反应方程式为:
CaFe(CO3)2  CaO+FeO+2CO2↑
CaO+FeO+2CO2↑
(2)一定条件下,气体二氧化碳与固体1中的某种成分可能发生氧化还原反应,可能的化学反应方程式:2FeO+CO2 Fe2O3+CO 检验方法:将固体用盐酸溶解,加入KSCN溶液,若溶液呈红色,证明有Fe(III);检测CO:将气体通入灼烧CuO,黑色固体变成红色。(3)综上分析,白色沉淀1是碳酸钙,其中的金属元素是20号Ca,其原子结构示意图为:
Fe2O3+CO 检验方法:将固体用盐酸溶解,加入KSCN溶液,若溶液呈红色,证明有Fe(III);检测CO:将气体通入灼烧CuO,黑色固体变成红色。(3)综上分析,白色沉淀1是碳酸钙,其中的金属元素是20号Ca,其原子结构示意图为:
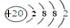 ;气体甲是CO2,其电子式为:
;气体甲是CO2,其电子式为: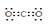 ;
;
(4)白色沉淀2在空气中变成红褐色沉淀的原因是4Fe(OH)2+O2+2H2O=4Fe(OH)3
【思路点拨】本题考查了物质的推断,注意寻找题目的突破口,大胆推测,题目有一定难度。

