海洋是个巨大的宝藏。人类利用海洋化学资源大体上经历了如图1所
海洋是个巨大的宝藏。人类利用海洋化学资源大体上经历了如图1所示几个阶段。
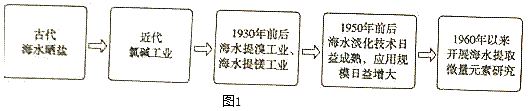
(1)海水经日晒蒸发水分,变为饱和溶液,再晒析出食盐,这一过程叫 蒸发结晶 ,这样得到的是“粗盐”,不仅含有泥沙,还含有Ca2+、SO42﹣、Mg2+等为去除三种杂质离子,可向粗盐水中依大加入过量的 (填化学式),过滤去除沉淀后再加入适量盐酸,将溶液调至中性。
(2)氯碱工业基本流程(图2):
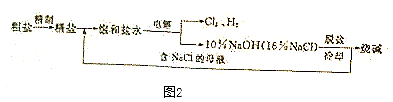
由图示可知工艺中可循环利用的物质是 。
(3)海水提镁流程:海水(MgCl2)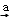 氢氧化镁
氢氧化镁 氧化镁
氧化镁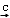 镁,写出其中任一个反应的化学方程式 ,提取氯化镁历经 a、b两步转换的目的是 。
镁,写出其中任一个反应的化学方程式 ,提取氯化镁历经 a、b两步转换的目的是 。
(4)下列方法中能淡化海水的是 (填字母)。
A.过滤法 B.沉淀法 C.多级闪急蒸馏法 D.分解法
解析(1)海水经日晒蒸发水分,变为饱和溶液,再晒析出食盐,这一过程是蒸发水分析出晶体,叫蒸发结晶,这样得到的是“粗盐”,含有Ca2+、SO42﹣、Mg2+等为去除三种杂质离子,要除去这些杂质离子,加入的试剂要注意后加入的试剂需要把先加入的过量的试剂除去,故可向粗盐水中依大加入过量的 BaCl2、NaOH、Na2CO3;过滤去除沉淀后再加入适量盐酸,将溶液调至中性。(2)根据图示可以看出,该工艺中可循环利用的物质是氯化钠。(3)海水提镁中氯化镁能与氢氧化钙反应生成氢氧化镁沉淀和氯化钙,化学方程式为MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2,提取氯化镁历经 a、b两步转换是为了获得比较纯净的氧化镁。(4)多级闪急蒸馏法能淡化海水。
答案(1)蒸发结晶;BaCl2、NaOH、Na2CO3
(2)NaCl
(3)MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2;获得比较纯净的氧化镁
(4)C

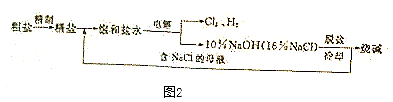
![]() 氢氧化镁
氢氧化镁![]() 氧化镁
氧化镁![]() 镁,写出其中任一个反应的化学方程式 ,提取氯化镁历经 a、b两步转换的目的是 。
镁,写出其中任一个反应的化学方程式 ,提取氯化镁历经 a、b两步转换的目的是 。