人工肾脏可用间接电化学方法除去代谢产物中的尿素(CO(NH2)2),原理如图.
(1)阳极室中发生的反应依次有: .
(2)电解结束后,阴极室溶液的pH与电解前相比将 ;若两极共收集到气体13.44L(标准状况),则除去的尿素为 g(忽略气体的溶解,下同).
(3)若关闭左下侧与左上侧溶液的导入导出,当电解过程中转移了2mol电子,则质子交换膜两侧电解液的质量变化差(△m左﹣△m右)为 g.
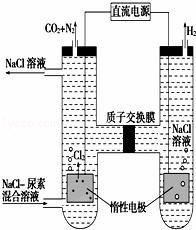
人工肾脏可用间接电化学方法除去代谢产物中的尿素(CO(NH2)2),原理如图.
(1)阳极室中发生的反应依次有: .
(2)电解结束后,阴极室溶液的pH与电解前相比将 ;若两极共收集到气体13.44L(标准状况),则除去的尿素为 g(忽略气体的溶解,下同).
(3)若关闭左下侧与左上侧溶液的导入导出,当电解过程中转移了2mol电子,则质子交换膜两侧电解液的质量变化差(△m左﹣△m右)为 g.

【考点】电解原理.
【分析】(1)阴极反应为:6H2O+6e﹣═6OH﹣+3H2↑(或6H++6e﹣═3H2↑),阳极反应为:6Cl﹣﹣6e﹣═3Cl2↑,CO(NH2)2+3Cl2+H2O═N2+CO2+6HCl;
(2)阴极反应为:6H2O+6e﹣═6OH﹣+3H2↑(或6H++6e﹣═3H2↑)阳极反应为:6Cl﹣﹣6e﹣═3Cl2↑,CO(NH2)2+3Cl2+H2O═N2+CO2+6HCl,根据上述反应式可以看出在阴、阳极上产生的OH﹣、H+的数目相等,阳极室中反应产生的H+通过质子交换膜进入阴极室与OH﹣恰好反应生成水,所以阴极室中电解前后溶液的pH不变;若两极共收集到气体13.44L(标准状况),混合气体物质的量=![]() =0.6mol,根据CO(NH2)2+3Cl2+H2O═N2+CO2+6HCl可知n(N2)=n(CO2)=0.6mol×
=0.6mol,根据CO(NH2)2+3Cl2+H2O═N2+CO2+6HCl可知n(N2)=n(CO2)=0.6mol×![]() =0.12 mol,根据N原子守恒计算尿素的物质的量,再根据m=nM计算尿素质量;
=0.12 mol,根据N原子守恒计算尿素的物质的量,再根据m=nM计算尿素质量;
(3)转移2mol电子时,阳极6Cl﹣﹣6e﹣═3Cl2↑,CO(NH2)2+3Cl2+H2O═N2+CO2+6HCl,阴极反应为:6H++6e﹣═3H2↑,所以质子交换膜左边的2mol氢离子进去右边,右侧氢离子放出氢气,质量不变;左侧阳极室中生成1molCl2,最终放出![]() molN2和
molN2和![]() molCO2,据此分析.
molCO2,据此分析.
【解答】解:(1)根据图知,阴极反应为:6H2O+6e﹣═6OH﹣+3H2↑(或6H++6e﹣═3H2↑),阳极反应为:6Cl﹣﹣6e﹣═3Cl2↑,CO(NH2)2+3Cl2+H2O═N2+CO2+6HCl,
故答案为:6Cl﹣﹣6e﹣═3Cl2↑;CO(NH2)2+3Cl2+H2O═N2+CO2+6HCl;
③阴极反应为6H2O+6e﹣═6OH﹣+3H2↑(或6H++6e﹣═3H2↑),阳极反应为6Cl﹣﹣6e﹣═3Cl2↑,CO(NH2)2+3Cl2+H2O═N2+CO2+6HCl,根据上述反应式可以看出在阴、阳极上产生的OH﹣、H+的数目相等,阳极室中反应产生的H+通过质子交换膜进入阴极室与OH﹣恰好反应生成水,所以阴极室中电解前后溶液的pH不变;若两极共收集到气体13.44L(标准状况),混合气体物质的量=![]() =0.6mol,根据CO(NH2)2+3Cl2+H2O═N2+CO2+6HCl可知n(N2)=n(CO2)=0.6mol×
=0.6mol,根据CO(NH2)2+3Cl2+H2O═N2+CO2+6HCl可知n(N2)=n(CO2)=0.6mol×![]() =0.12 mol,根据N原子守恒得n[CO(NH2)2]=n(N2)=0.12mol,尿素质量m=nM=0.12mol×60g/mol=7.2g,
=0.12 mol,根据N原子守恒得n[CO(NH2)2]=n(N2)=0.12mol,尿素质量m=nM=0.12mol×60g/mol=7.2g,
故答案为:不变;7.2;
(3)转移2mol电子时,阳极6Cl﹣﹣6e﹣═3Cl2↑,CO(NH2)2+3Cl2+H2O═N2+CO2+6HCl,阴极反应为:6H++6e﹣═3H2↑,所以质子交换膜左边的2mol氢离子进去右边,右侧氢离子放出氢气,质量不变;左侧阳极室中生成1molCl2,最终放出![]() molN2和
molN2和![]() molCO2,故膜两侧电解液的质量变化差(△m左﹣△m右)=
molCO2,故膜两侧电解液的质量变化差(△m左﹣△m右)=![]() (28+44)=24g,
(28+44)=24g,
故答案为:24.
【点评】本题考查化学电源新型电池、电解原理等知识点,明确各个电极上发生的反应是解本题关键,难点是电极反应式的书写及有关计算,书写电极反应式要结合电解质溶液酸碱性书写,注意(3)中阳极上所发生的反应,为易错点.