жҺўз©¶дёҖж°§еҢ–зўізҡ„жҖ§иҙЁе’Ңз”ЁйҖ”
еӯҰж ЎеҢ–еӯҰе…ҙи¶Је°Ҹз»„зҡ„еҗҢ еӯҰеҜ№дёҖд»ҪеӣәдҪ“ж ·е“ҒиҝӣиЎҢдәҶжҺўз©¶пјҺйҖҡиҝҮе®һйӘҢе·ІзЎ®е®ҡиҜҘж ·е“Ғз”ұж°§еҢ–й“ңе’Ңй“ңзІүж··еҗҲиҖҢжҲҗпјҺ他们称еҸ–дәҶ20gеӣәдҪ“ж ·е“ҒпјҢз”Ёеӣҫ1жүҖзӨәзҡ„иЈ…зҪ®з»§з»ӯе®һйӘҢпјҢиҮіеҸҚеә”е®Ңе…ЁжөӢе®ҡзҡ„йғЁеҲҶж•°еӣҫ2жүҖзӨәпјҺ

жҚ®еӣҫи§ЈеҶіжңүе…ій—®йўҳпјҡ
пјҲ1пјүеҶҷеҮәеӣҫ1дёӯзЎ¬иҙЁзҺ»з’ғз®ЎдёӯеҸ‘з”ҹзҡ„еҢ–еӯҰж–№зЁӢејҸгҖҖгҖҖпјӣе№ҝеҸЈз“¶дёӯзҡ„зҺ°иұЎжҳҜгҖҖгҖҖпјӣеӣҫ1е®һйӘҢдёӯеӯҳеңЁзҡ„жҳҺжҳҫзјәйҷ·жҳҜгҖҖгҖҖпјҺ
пјҲ2пјүеӣҫ2дёӯMзӮ№иЎЁзӨәеҸҚеә”гҖҖгҖҖпјҲеЎ«вҖңиҝӣиЎҢдёӯвҖқжҲ–вҖңз»“жқҹвҖқпјүпјҢеӣҫ2 дёӯ16.8е…Ӣзү©иҙЁжҳҜгҖҖгҖҖпјҲеЎ«зү©иҙЁеҗҚз§°пјү
пјҲ3пјүеҺҹж··еҗҲзү©дёӯж°§еҢ–й“ңзҡ„иҙЁйҮҸжҳҜгҖҖгҖҖе…ӢпјҺ
пјҲ4пјүеҒҮеҰӮдә§з”ҹзҡ„дәҢж°§еҢ–зўіе…ЁйғЁиў«жҫ„жё…зҡ„зҹізҒ°ж°ҙеҗёж”¶пјҢдә§з”ҹзҡ„жІүж·ҖжҳҜеӨҡе°‘е…ӢпјҹпјҲеҶҷеҮәи®Ўз®—иҝҮзЁӢпјү
гҖҖ
гҖҗиҖғзӮ№гҖ‘дёҖж°§еҢ–зўізҡ„еҢ–еӯҰжҖ§иҙЁпјӣд№ҰеҶҷеҢ–еӯҰж–№зЁӢејҸпјӣж №жҚ®еҢ–еӯҰеҸҚеә”ж–№зЁӢејҸзҡ„и®Ўз®—пјҺ
гҖҗдё“йўҳгҖ‘зўіеҚ•иҙЁдёҺеҗ«зўіеҢ–еҗҲзү©зҡ„жҖ§иҙЁдёҺз”ЁйҖ”пјҺ
гҖҗеҲҶжһҗгҖ‘пјҲ1пјүдёҖж°§еҢ–зўіиҝҳеҺҹж°§еҢ–й“ңз”ҹжҲҗй“ңе’ҢдәҢж°§еҢ–зўіпјҢжҚ®жӯӨд№ҰеҶҷеҢ–еӯҰж–№зЁӢејҸпјҢдәҢж°§еҢ–зўіиғҪдҪҝжҫ„жё…зҹізҒ°ж°ҙеҸҳжө‘жөҠпјҢдёҖж°§еҢ–зўіжңүжҜ’иҰҒеӨ„зҗҶйҳІжӯўжұЎжҹ“з©әж°”пјӣ
пјҲ2пјүж №жҚ®зӮ№MеҗҺзү©иҙЁиҙЁйҮҸдёҚеҸҳеҲҶжһҗпјӣ
пјҲ3пјүж №жҚ®еҸҚеә”еүҚеҗҺеӣәдҪ“иҙЁйҮҸеҮҸе°‘пјҢжұӮеҮәж··еҗҲзү©дёӯж°§еҢ–й“ңзҡ„иҙЁйҮҸпјӣ
пјҲ4пјүж №жҚ®дәҢж°§еҢ–зўіе’Ңжҫ„жё…зҹізҒ°ж°ҙеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸиҝӣиЎҢи®Ўз®—пјҺ
гҖҗи§Јзӯ”гҖ‘и§ЈпјҡпјҲ1пјүдёҖж°§еҢ–зўіжңүиҝҳеҺҹжҖ§еҸҜд»Ҙе°Ҷй“ңд»Һе…¶ж°§еҢ–зү©дёӯиҝҳеҺҹеҮәжқҘпјҢеҸ‘з”ҹеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸдёәпјҡCO+CuO
 Cu+CO2пјӣдёҖж°§еҢ–зўіиҝҳеҺҹж°§еҢ–й“ңеҗҺз”ҹжҲҗдәҢж°§еҢ–зўіе’Ңй“ңпјҢдәҢж°§еҢ–зўіиғҪдҪҝжҫ„жё…зҹізҒ°ж°ҙеҸҳжө‘жөҠпјҢжІЎеҸҚеә”е®Ңзҡ„дёҖж°§еҢ–зўіиҰҒеӨ„зҗҶд»ҘйҳІжұЎжҹ“з©әж°”пјҢж•…еЎ«пјҡCO+CuO
Cu+CO2пјӣдёҖж°§еҢ–зўіиҝҳеҺҹж°§еҢ–й“ңеҗҺз”ҹжҲҗдәҢж°§еҢ–зўіе’Ңй“ңпјҢдәҢж°§еҢ–зўіиғҪдҪҝжҫ„жё…зҹізҒ°ж°ҙеҸҳжө‘жөҠпјҢжІЎеҸҚеә”е®Ңзҡ„дёҖж°§еҢ–зўіиҰҒеӨ„зҗҶд»ҘйҳІжұЎжҹ“з©әж°”пјҢж•…еЎ«пјҡCO+CuO
 Cu+CO2пјӣжҫ„жё…зҹізҒ°ж°ҙеҸҳжө‘жөҠпјӣжІЎжңүе°ҫж°”еӨ„зҗҶиЈ…зҪ®пјӣ
Cu+CO2пјӣжҫ„жё…зҹізҒ°ж°ҙеҸҳжө‘жөҠпјӣжІЎжңүе°ҫж°”еӨ„зҗҶиЈ…зҪ®пјӣ
пјҲ2пјүз”ұеӣҫ2дёӯMзӮ№д»ҘеҗҺеӣәдҪ“иҙЁйҮҸдёҚеҶҚеҮҸе°ҸпјҢиҜҙжҳҺеңЁMзӮ№ж—¶еҸҚеә”з»“жқҹпјҢз”ұеҸҚеә”з”ҹжҲҗзү©жҳҜй“ңпјҢжүҖд»Ҙеү©дҪҷзҡ„16.8gзү©иҙЁжҳҜй“ңпјӣж•…еЎ«пјҡз»“жқҹпјӣй“ңпјӣ
пјҲ3пјүж №жҚ®20gеӣәдҪ“еҮҸе°‘иҮі16.8gеҮҸе°‘дәҶ3.2gпјҢеҮҸе°‘зҡ„иҙЁйҮҸжҳҜж°§еҢ–й“ңдёӯеҗ«жңүзҡ„ж°§е…ғзҙ пјҢжҚ®жӯӨеҸҜзҹҘеҺҹж°§еҢ–й“ңзҡ„иҙЁйҮҸдёәпјҡ3.2g
 =16gпјӣж•…еЎ«пјҡ16пјӣ
=16gпјӣж•…еЎ«пјҡ16пјӣ
пјҲ4пјүи§Јпјҡи®ҫдә§з”ҹзҡ„дәҢж°§еҢ–зўізҡ„иҙЁйҮҸдёәxпјҢз”ҹжҲҗCaCO3иҙЁйҮҸдёәy
CO+CuO
 Cu+CO2
Cu+CO2
80В В В В В В В В В В В В В В 44
В В В В В 16gВ В В В В В В x


и§Јж–№зЁӢx=8.8g
CO2+CaпјҲOHпјү2в•җCaCO3вҶ“+H2O
44В В В В В В В В В В В В 100
8.8gВ В В В В В В В В В В В y
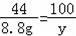

и§Јж–№зЁӢy=20g
зӯ”пјҡз”ҹжҲҗжІүж·ҖиҙЁйҮҸдёә20gпјҺ
гҖҗзӮ№иҜ„гҖ‘жң¬йўҳиҖғжҹҘдёҖж°§еҢ–зўізҡ„иҝҳеҺҹжҖ§д»ҘеҸҠе…ідәҺеҢ–еӯҰеҸҚеә”ејҸзҡ„и®Ўз®—пјҢйңҖиҰҒеҗҢеӯҰ们иғҪеӨҹеҮҶзЎ®зҡ„д№ҰеҶҷеҢ–еӯҰж–№зЁӢејҸпјҢзҗҶжё…зү©иҙЁй—ҙзҡ„е…ізі»пјҢ并жңүиҫғејәзҡ„еҲҶжһҗиғҪеҠӣе’Ңи®Ўз®—иғҪеҠӣпјҢжүҚеҸҜеҒҡеҮәеҮҶзЎ®зҡ„и®Ўз®—пјҺ
гҖҖ


