某同学进行中和反应实验:取适量的NaOH溶液于烧杯中,滴加几滴紫色石蕊试液,再逐渐滴加稀H2SO4,测得溶液的pH及颜色变化情况如表:
| 滴加稀H2S04的体积/mI, | O | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| pH | 13.0 | 12.8 | 12.5 | 12.2 | 7.0 | 2.0 | 1.7 | 1.6 |
| 溶液颜色 | 蓝色 | 紫色 | 红色 |
(1)如图中符合上述实验过程的图形是
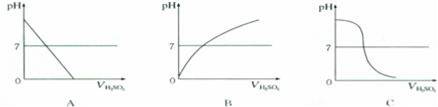

(2)当加入4mL稀H2SO4时,溶液显 性,溶液中的溶质为 .
(3)写出该中和反应的化学方程式: .
【考点】中和反应及其应用;溶液的酸碱性与pH值的关系;常见化学反应中的质量关系.
【专题】常见的酸 酸的通性.
【分析】氢氧化钠溶液呈碱性,其溶液的酸碱度大于7;硫酸溶液呈酸性,溶液的酸碱度小于7;二者进行混合时发生中和反应,混合溶液的酸碱度逐渐接近中性,在恰好完全反应时,所得溶液酸碱度恰好等于7为中性;随后加入的稀硫酸会使溶液的酸碱度逐渐减小.
【解答】解:(1)由实验的数据表,该变化过程中溶液由碱性逐渐变成中性,待稀硫酸过量,溶液的酸性继续增大,溶液的酸碱度则继续减小;因此图C可以正确表示这一变化特点;
(2)当加入4mL稀H2SO4时,溶液酸碱度等于7,溶液呈中性,此时氢氧化钠与硫酸恰好完全反应,生成硫酸钠和水;故此时溶液中溶质为硫酸钠;
(3)氢氧化钠与硫酸发生中和反应,通过交换成分生成硫酸钠和水,反应的化学方程式为2NaOH+H2SO4═Na2SO4+2H2O.
故答案为:
(1)C;
(2)中;硫酸钠;
(3)2NaOH+H2SO4═Na2SO4+2H2O.
【点评】酸碱中和时,溶液的酸碱度会随反应的不断进行而发生变化,明确两种溶液滴加顺序,对于判断溶液酸碱度变化的判断是关键.


