(1)NaHSO
4溶于水的电离方程式为____________________,NaHSO
4受热熔化的电离方程式为__________________________________。
(2)向NaHSO4溶液中分别加入下列物质,写出化学反应的离子方程式,标明是否为氧化还原反应(只写出“是”或“否”即可)。
①Ba(NO3)2溶液_____________________________,__________。
②Na2CO3溶液______________________________,__________。
③Zn__________________________________,_____________。
④Cu(OH)2________________________________,___________。
⑤Ba(OH)2________________________________,___________。
(1)NaHSO4====Na++H++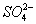 NaHSO4====Na++
NaHSO4====Na++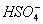
(2)①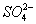 +Ba2+====BaSO4↓ 否
+Ba2+====BaSO4↓ 否
②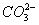 +2H+====CO2↑+H2O 否
+2H+====CO2↑+H2O 否
③Zn+2H+====Zn2++H2↑ 是
④Cu(OH)2+2H+====Cu2++2H2O 否
⑤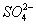 +H++Ba2++OH-====BaSO4↓+H2O 否
+H++Ba2++OH-====BaSO4↓+H2O 否
或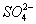 +2H++Ba2++2OH-====BaSO4↓+2H2O 否
+2H++Ba2++2OH-====BaSO4↓+2H2O 否
解析:(1)NaHSO4是二元强酸的酸式盐,易溶易电离。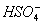 在水溶液里还易电离,但在熔化状态下不能电离。
在水溶液里还易电离,但在熔化状态下不能电离。
(2)NaHSO4溶于水电离出Na+、H+、 等三种离子,在溶液里,Na+一般不发生化学反应,而H+、
等三种离子,在溶液里,Na+一般不发生化学反应,而H+、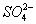 等离子易与某些离子或分子发生化学反应。
等离子易与某些离子或分子发生化学反应。
