将稀硫酸慢慢滴入盛有氢氧化钠溶液的烧杯中,用温度计测量烧杯中溶液的温度,温度随加入稀硫酸的质量变化曲线如图所示:
(1)写出该反应的化学方程式: .
(2)由图可知,稀硫酸与氢氧化钠溶液发生的反应是 (填“放热”或“吸热”)反应.
(3)B点溶液中含有的溶质是 ,C点的pH (填“>”“=”或“<”)7.
(4)生石灰溶于水也会放出热量,使生石灰溶于水放出热量的原因是 (用化学方程式表示)
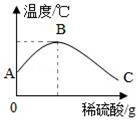

将稀硫酸慢慢滴入盛有氢氧化钠溶液的烧杯中,用温度计测量烧杯中溶液的温度,温度随加入稀硫酸的质量变化曲线如图所示:
(1)写出该反应的化学方程式: .
(2)由图可知,稀硫酸与氢氧化钠溶液发生的反应是 (填“放热”或“吸热”)反应.
(3)B点溶液中含有的溶质是 ,C点的pH (填“>”“=”或“<”)7.
(4)生石灰溶于水也会放出热量,使生石灰溶于水放出热量的原因是 (用化学方程式表示)


【考点】97:中和反应及其应用;8L:生石灰的性质与用途;99:溶液的酸碱性与pH值的关系;G5:书写化学方程式、.
【分析】(1)根据反应的原理以及化学方程式的写法来分析;
(2)根据图象可以看出随着硫酸的加入温度在逐渐上升,据此进行分析解答;
(3)根据不同溶液的温度来分析;
(4)根据反应的原理来分析解答.
【解答】解:(1)氢氧化钠与硫酸反应生成硫酸钠和水;故填:2NaOH+H2SO4=Na2SO4+2H2O;
(2)由图象可以看出,随着稀硫酸的加入,温度在逐渐的升高,说明稀硫酸与氢氧化钠溶液发生的反应是放热反应.故填:放热;
(3)由图是可知,在B点前后温度是两种情况,B点温度最高,B点表示酸碱恰好完全反应,反应后生成硫酸钠和水,显中性;C点表示的溶液中硫酸已经过量,此时溶液的pH<7;故填:硫酸钠;<;
(4)生石灰与水反应生成熟石灰,此过程会放出大量的热,故填:CaO+H2O=Ca(OH)2.