稀硫酸与氢氧化钠溶液混合没有明显现象,为证明硫酸与氢氧化钠发生了化学反应,小颖同学进行了如下探究:
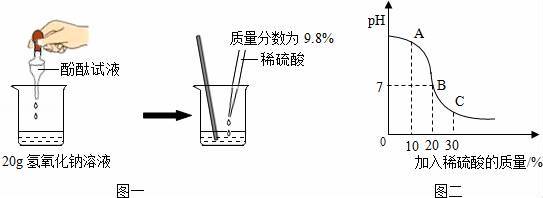

(1)小颖同学通过图一所示的实验,证明硫酸与氢氧化钠发生了化学反应,她依据的实验现象是 .
(2)氢氧化钠是实验室常用药品,下列相关说法中,正确的是 (填序号).
A.称量:可将NaOH固体直接放在天平左边托盘的纸上进行称量
B.溶解:NaOH固体溶于水时放出大量热,溶解时需用玻璃棒不断搅拌
C.应急:先用大量水冲洗皮肤上的NaOH溶液,再涂上3%~5%稀盐酸溶液
D.保存:NaOH固体易吸收空气中的水蒸气和CO2,应密封保存
(3)溶液的pH与加入稀硫酸的质量关系如图二所示,图中A点对应溶液中的溶质有 (写化学式)
(4)根据图示信息,当溶液恰好为中性时,求所得不饱和溶液中溶质的质量.(不计滴加的酚酞试液质量,计算精确到0.01g)
【考点】G6:根据化学反应方程式的计算;97:中和反应及其应用;99:溶液的酸碱性与pH值的关系.
【分析】(1)根据酸和碱使酚酞试液的变色情况和考虑;
(2)A、根据氢氧化钠具有强烈的腐蚀性进行分析;
B、根据溶解时要用玻璃棒不断搅拌分析;
C、根据碱溶液粘在皮肤上,先用较多水冲洗,再涂上硼酸溶液进行解答;
D、根据已有的氢氧化钠的性质进行分析解答,氢氧化钠具有吸水性和与二氧化碳反应的性质.
(3)根据A点溶液p大于7分析解答;
(4)根据硫酸的质量结合方程式求解硫酸钠的质量.
【解答】解:(1)氢氧化钠显碱性,能使酚酞试液变为红色,硫酸与氢氧化钠反应生成硫酸钠和水,硫酸钠显中性,不能使酚酞试液变红,所以溶液由红色变为无色;
(2)A、氢氧化钠具有强烈的腐蚀性,不能放在纸片上称量,应放在烧杯等玻璃器皿中称量,故A错误;
B、溶解时要用玻璃棒不断搅拌,加速溶解,故B正确;
C、当氢氧化钠溶液溅到皮肤上时,应该立即用大量的水冲洗,然后再涂上3%~5%硼酸溶液,而稀盐酸具有腐蚀性,故C错误;
D、氢氧化钠具有吸水性,能与空气中的二氧化碳反应而变质,故需要密封保存,故D正确;
故选:BD;
(3)由图示可知,在a点时溶液的pH大于7,说明NaOH过量,硫酸完全反应,没有剩余,所以溶液中含有的溶质有:Na2SO4、NaOH;
(4)H2SO4质量=20g×9.8%=1.96 g
设Na2SO4质量为 x,
H2SO4+2NaOH=Na2SO4+2H2O
98 142
1.96g x
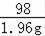
 =
=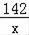

x=2.84g
答:所得溶液中含有硫酸钠 2.84g
故答案为:(1)溶液由红色变为无色;
(2)BD;
(3)NaOH、Na2SO4;
(4)所得溶液中含有2.84gNa2SO4.
【点评】本题考查了酸碱中和反应时溶液PH的变化以及反应时物质之间的质量关系,完成此题,可以依据已有的知识以及图示进行.所以要求同学们在平时的学习中加强课本基础知识的储备,以便能够灵活应用.


