某同学取一定量的Al、Fe混合物,与2.0L极稀的HNO3充分反应,假设HNO3的还原产物全部为铵盐.在反应后的溶液中,逐滴加入4mol•L﹣1的NaOH溶液,所加NaOH溶液的体积与产生的沉淀的物质的量的关系如图所示.分析图象回答问题:
(1)OC段和DE段发生反应的离子方程式分别为:OC段: ;DE段: .
(2)请写出任意一个Al、Fe与极稀HNO3反应的化学方程式: .
(3)B与A的差值为 mol.
(4)B点对应的沉淀的物质的量为 mol,C点对应的氢氧化钠溶液的体积为 mL.
(5)原硝酸溶液的物质的量浓度为 mol/L.

【考点】有关混合物反应的计算;镁、铝的重要化合物.
【专题】图像图表题.
【分析】铝粉和铁粉的混合物与一定量很稀HNO3充分反应,被氧化为Al3+、Fe3+,假设HNO3的还原产物全部为铵盐.由图可得硝酸过量,加入氢氧化钠溶液应先与硝酸反应,再生成沉淀,当沉淀完全后,由图知继续加入氢氧化钠溶液,沉淀量不变,可得与NH4+发生了反应,则随着NaOH的滴加,发生的反应依次有:
①H++OH﹣=H2O,②Fe3++3OH﹣=Fe(OH)3↓,Al3++3OH﹣=Al(OH)3↓,③NH4++OH﹣═NH3•H2O,④Al(OH)3 +OH﹣=AlO2﹣+2H2O,
B与A的差值为氢氧化铝的物质的量,计算EF段消耗的氢氧化钠,根据Al(OH)3 +OH﹣=AlO2﹣+2H2O,得出Al(OH)3的物质的量;
根据DE段消耗的氢氧化钠计算溶液中n(NH4+),结合Al(OH)3的物质的量,再根据电子转移守恒,计算Fe的物质的量;
B点对应的沉淀为Al(OH)3、Fe(OH)3,根据Al、Fe守恒计算其物质的量;
由反应过程可知,到加入氢氧化钠为31mL时,溶液中溶质为硝酸钠与硝酸铵,根据钠元素守恒计算硝酸钠,结合n(NH4+)可得n(NH4NO3),根据氮元素守恒可知:原硝酸溶液中n(HNO3)=n(NaNO3)+2n(NH4NO3),而c点溶液为NaNO3、NH4NO3、Fe(NO3)3、Al(NO3)3,根据氮元素守恒计算c点溶液中n′(NaNO3),进而计算c点NaOH的物质的量,据此解答.
【解答】解:铝粉和铁粉的混合物与一定量很稀HNO3充分反应,被氧化为Al3+、Fe3+,假设HNO3的还原产物全部为铵盐.由图可得硝酸过量,加入氢氧化钠溶液应先与硝酸反应,再生成沉淀,当沉淀完全后,由图知继续加入氢氧化钠溶液,沉淀量不变,可得与NH4+发生了反应,则随着NaOH的滴加,发生的反应依次有:
①H++OH﹣=H2O,②Fe3++3OH﹣=Fe(OH)3↓,Al3++3OH﹣=Al(OH)3↓,③NH4++OH﹣═NH3•H2O,④Al(OH)3 +OH﹣=AlO2﹣+2H2O,
(1)OC段发生离子方程式为:H++OH﹣=H2O;DE段发生离子方程式为NH4++OH﹣=NH3•H2O,故答案为:H++OH﹣=H2O;NH4++OH﹣=NH3•H2O;
(2)任意一个Al、Fe与极稀HNO3反应的化学方程式为:8Al+30HNO3=8Al(NO3)3+3NH4NO3+9H2O或8Fe+30HNO3=8 Fe (NO3)3+3NH4NO3+9H2O,
故答案为:8Al+30HNO3=8Al(NO3)3+3NH4NO3+9H2O或8Fe+30HNO3=8 Fe (NO3)3+3NH4NO3+9H2O;
(3)B与A的差值为氢氧化铝的物质的量,由图可知,EF段消耗的氢氧化钠溶液为36mL﹣34m=2mL,故该阶段参加反应的氢氧化钠为0.002L×4mol/L=0.008mol,根据Al(OH)3 +OH﹣=AlO2﹣+2H2O可知,Al(OH)3的物质的量为0.008mol,
故答案为:0.008;
(4)由图可知,DE段消耗的氢氧化钠的体积为34mL﹣31m=3mL,故该阶段参加反应的氢氧化钠为0.003L×4mol/L=0.012mol,根据NH4++OH﹣═NH3•H2O 可知,计算溶液中n(NH4+)=0.012ml,根据(3)中计算可知n[Al(OH)3]=0.008mol,根据铝元素守恒,故混合金属中n(Al)=0.008mol,根据电子转移守恒有,3n(Fe)+3n(Al)=8n(NH4+),即3n(Fe)+3×0.008mol=8×0.012mol,解得n(Fe)=0.024mol,可知n[Fe(OH)3]=n(Fe)=0.024mol,B点对应的沉淀Al(OH)3、Fe(OH)3,二者的物质的量之和=0.008mol+0.024mol=0.032mol;
由反应过程可知,到加入氢氧化钠为31mL时,溶液中溶质为硝酸钠与硝酸铵,n(NH4NO3)=n(NH4+)=0.012mol,根据钠元素守恒,可知n(NaNO3)=n(NaOH)=0.031L×4mol/L=0.124mol,根据氮元素守恒可知,原硝酸溶液中n(HNO3)=n(NaNO3)+2n(NH4NO3)=0.124mol+0.012mol×2=0.148mol,而c点溶液为NaNO3、NH4NO3、Fe(NO3)3、Al(NO3)3,根据氮元素守恒n′(NaNO3)+2n(NH4NO3)+3n[Fe(NO3)3]+3n[Al(NO3)3]=n(HNO3),故c点溶液中n′(NaNO3)=0.148mol﹣0.012mol×2﹣0.024mol×3﹣0.008mol×3=0.028mol,故c点加入NaOH的物质的量=0.028mol,c点NaOH溶液的体积=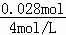 =0.007L=7 mL,
=0.007L=7 mL,
故答案为:0.032;7;
(5)根据(4)中计算可知,原硝酸溶液中n(HNO3)=0.148mol,则原硝酸溶液的物质的量浓度为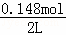 =0.074mol/L,故答案为:0.074.
=0.074mol/L,故答案为:0.074.
【点评】本题以图象形式,考查金属与硝酸的反应、混合物计算等,清楚图中各阶段反应过程是解题的关键,解答中注意守恒思想的运用,题目过程复杂,计算量大,侧重对学生分析解决问题能力、计算能力的考查,为易错题目,难度较大.

