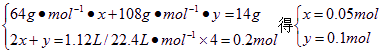(1)在浓硝酸中放入铜片。
①开始反应的化学方程式为__________________________________。
②若铜有剩余,则反应将要结束时的反应方程式是______________________________。
③等反应停止后,再加入少量25%的稀硫酸,这时铜片上又有气泡产生,其原因是
_______________________________________________________________________________。
(2)在100 mL混合酸中,c(HNO3)=0.4 mol·L-1,c(H2SO4)=0.2 mol·L-1,向其中加入2.56 g铜粉,微热,等充分反应后,溶液中Cu2+的物质的量浓度为__________________________。
(3)14 g铜银合金与一定量某浓度的硝酸溶液反应,将放出的气体与1.12 L(标准状况下)氧气混合通入水中,恰好全部被水吸收,则合金中铜的质量是_________________g。
(1)①Cu+4HNO3(浓)====Cu(NO3)2+2NO2↑+2H2O(2分)
②3Cu+8HNO3(稀)====3Cu(NO3)2+2NO↑+4H2O(2分)
③H+与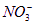 形成了稀HNO3溶液,又与过量的铜反应产生NO气体(2分)
形成了稀HNO3溶液,又与过量的铜反应产生NO气体(2分)
(2)0.3 mol·L-1(3分) (3)3.2(3分)
解析:
(1)开始时铜与浓硝酸发生反应,Cu+4HNO3====Cu(NO3)2+2NO2↑+2H2O,结束时,铜与稀HNO3反应,方程式为:3Cu+8HNO3====3Cu(NO3)2+2NO↑+4H2O,反应停止后,再加入稀H2SO4,H+与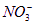 构成了氧化性条件,发生3Cu+2
构成了氧化性条件,发生3Cu+2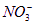 +8H+====3Cu2++2NO↑+4H2O。
+8H+====3Cu2++2NO↑+4H2O。
(2)解:n(Cu)=2.56 g/64 g·mol-1=0.04 mol,n(H+)=0.4 mol·L-1×0.1 L+0.2 mol·L-1×0.1 L×2=0.08 mol,n(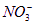 )=0.4 mol·L-1×0.1 L=0.04 mol
)=0.4 mol·L-1×0.1 L=0.04 mol
根据:3Cu+2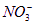 +8H+====3Cu2++2NO↑+4H2O知:溶液中n(H+)少量,所以按H+的物质的量计算。生成n(Cu2+)=0.08 mol×
+8H+====3Cu2++2NO↑+4H2O知:溶液中n(H+)少量,所以按H+的物质的量计算。生成n(Cu2+)=0.08 mol× =0.03 mol,则c(Cu2+)=0.03 mol/0.1 L=0.3 mol·L-1
=0.03 mol,则c(Cu2+)=0.03 mol/0.1 L=0.3 mol·L-1
(3)根据题意,其反应过程为:
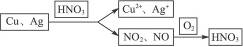
所以整个过程中14 g Cu、Ag失去电子数等于0.5 mol O2得到的电子数。
设Cu和Ag的物质的量分别为x、y。
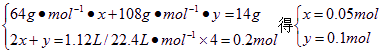
铜的质量为:m(Cu)=64 g·mol-1×0.05 mol=3.2 g