粗盐中含有难溶性杂质(泥沙等)和多种可溶性杂质(氯化镁、氯化钙等).某班同学在粗盐提纯实验中,为把少量可溶性杂质CaCl2,MgCl2一并除去,将教材中实验方案修改设计如下,请据此回答问题: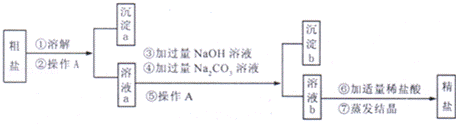
(1)实验操作A的名称是 ,该操作的目的是.
(2)写出步骤③中发生反应的主要化学方程式-------;步骤⑥的作用======.
(3)小刚同学认为该方案实际得到的氯化钠可能比粗盐中含有的氯化钠要多,请你为他找出理由: .
粗盐中含有难溶性杂质(泥沙等)和多种可溶性杂质(氯化镁、氯化钙等).某班同学在粗盐提纯实验中,为把少量可溶性杂质CaCl2,MgCl2一并除去,将教材中实验方案修改设计如下,请据此回答问题:
(1)实验操作A的名称是 ,该操作的目的是.
(2)写出步骤③中发生反应的主要化学方程式-------;步骤⑥的作用======.
(3)小刚同学认为该方案实际得到的氯化钠可能比粗盐中含有的氯化钠要多,请你为他找出理由: .
考点:
氯化钠与粗盐提纯;过滤的原理、方法及其应用;盐的化学性质;书写化学方程式、文字表达式、电离方程式.
专题:
常见的盐 化学肥料.
分析:
(1)根据过滤操作的目的解答;
(2)根据要求正确书写化学方程式,步骤⑥加适量稀盐酸的作用是除去过量的氢氧化钠和碳酸钠;
(3)根据实验过程中各步反应的生成物解答;
解答:
解:(1)实验操作X的名称是过滤,该操作的目的是除去难溶性杂质.
(2)实验步骤③的主要目的是除去氯化镁,氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠,反应的化学方程式为:
MgCl2+2NaOH═Mg(OH)2↓+2NaCl.步骤⑥加适量稀盐酸的作用是除去过量的氢氧化钠和碳酸钠;
(3)因为在实验过程中有氯化钠生成,故该方案实际得到的氯化钠可能比粗盐中含有的氯化钠要多.
答案:(1)过滤,除去难溶性杂质;
(2)MgCl2+2NaOH═Mg(OH)2↓+2NaCl,除去过量的氢氧化钠和碳酸钠;
(3)因为在实验过程中有氯化钠生成.
点评:
本题涉及除杂、化学方程式的书写、等方面的知识,难度适中,是综合性题目.[来源:]