元素周期表是学习化学的重要工具,它隐含着许多信息和规律.下表所列是五种短周期的原子半径及主要化合价(已知铍的原子半径为0.089nm)
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.16 | 0.143 | 0.102 | 0.099 | 0.074 |
| 主要化合价 | +2 | +3 | +6、﹣2 | ﹣1 | ﹣2 |
(1)A和E两元素组成的化合物的电子式 .
(2)B的最高价氧化物的水化物与C的最高价氧化物的水化物反应的离子方程式为:
(3)上述五种元素的最高价氧化物对应水化物的酸性最强的是 (填化学式)
(4)C和E形成的化合物中具有还原性的是 (填化学式).
(填化学式).
(5)A和D所形成化合物的晶体类型: .
1)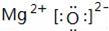 ;
;
(2)Al(OH)3+3H+=Al3+3H2O;
(3)HClO4;
(4)SO2;
(5)离子晶体.
【解析】
试题分析:短周期元素中,C、E都有﹣2价,处于ⅥA族,C有+6价且原子半径C>E,故C为硫、E为氧;D有﹣1价,原子半径大于氧,故D为Cl;A、B化合价分别为+2、+3,分别处于ⅡA族、ⅢA族,原子半径A>B>硫,故A为Mg、B为Al,据此解答.
解:短周期元素中,C、E都有﹣2价,处于ⅥA族,C有+6价且原子半径C>E,故C为硫、E为氧;D有﹣1价,原子半径大于氧,故D为Cl;A、B化合价分别为+2、+3,分别处于ⅡA族、ⅢA族,原子半径A>B>硫,故A为Mg、B为Al.
(1)A和E两元素组成的化合物为MgO,电子式为: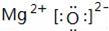 ,故答案为:
,故答案为: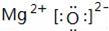 ;
;
(2)B的最高价氧化物的水化物为Al(OH)3,C的最高价氧化物的水化物为H2SO4,二者反应的离子方程式为:Al(OH)3+3H+=Al3+3H2O,故答案为:Al(OH)3+3H+=Al3+3H2O;
(3)上述五种元素中Cl的非金属性最强,故最高价氧化物对应水化物的酸性最强的是 HClO4,故答案为:HClO4;
(4)C和E形成的化合物中具有还原性的是SO2,故答案为:SO2;
(5)A和D所形成化合物为MgCl2,属于离子晶体,故答案为:离子晶体.
![]() (填化学式).
(填化学式).