й“ҒгҖҒй“ңж··еҗҲзІүжң«18.0gеҠ е…ҘеҲ°100mL 5.0molвҖўLп№Ј1 FeCl3жә¶ж¶ІдёӯпјҢе……еҲҶеҸҚеә”еҗҺпјҢеү©дҪҷеӣәдҪ“иҙЁйҮҸдёә2.8gпјҺдёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜ
A. еү©дҪҷеӣәдҪ“жҳҜй“ҒгҖҒй“ңж··еҗҲзү©
B. еҺҹеӣәдҪ“ж··еҗҲзү©дёӯй“ңзҡ„иҙЁйҮҸжҳҜ9.6g
C. еҸҚеә”еҗҺжә¶ж¶ІдёӯnпјҲFe3+пјү=0.10mol
D. еҸҚеә”еҗҺжә¶ж¶ІдёӯnпјҲFe2+пјү+nпјҲCu2+пјү=0.75mol
гҖҗзӯ”жЎҲгҖ‘D
гҖҗи§ЈжһҗгҖ‘
гҖҗеҲҶжһҗгҖ‘
й“ҒжҜ”й“ңжҙ»жіјпјҢдёҺFeCl3жә¶ж¶ІеҸҚеә”ж—¶е…ҲеҗҺеҸ‘з”ҹFe+2Fe3+=3Fe2+гҖҒCu+2Fe3+=Cu2++2Fe2+пјҢеҺҹж°ҜеҢ–й“Ғжә¶ж¶Ідёӯеҗ«жңүж°ҜеҢ–й“Ғзҡ„зү©иҙЁзҡ„йҮҸдёәn(FeCl3)=5mol/LГ—0.1L=0.5molпјҢз»“еҗҲеҸҚеә”зҡ„ж–№зЁӢејҸи§Јзӯ”гҖӮ
гҖҗиҜҰи§ЈгҖ‘й“Ғзҡ„иҝҳеҺҹжҖ§ејәдәҺй“ңпјҢжҠҠй“ҒгҖҒй“ңж··еҗҲзІүжң«еҠ е…Ҙж°ҜеҢ–й“Ғжә¶ж¶ІдёӯпјҢй“Ғе…ҲдёҺй“ҒзҰ»еӯҗеҸҚеә”пјҢж°ҜеҢ–й“Ғзҡ„зү©иҙЁзҡ„йҮҸжҳҜ0.5molпјҢ
и®ҫ0.5molй“ҒзҰ»еӯҗе®Ңе…ЁеҸҚеә”ж¶ҲиҖ—й“ҒгҖҒй“ңзҡ„иҙЁйҮҸеҲҶеҲ«дёәm1гҖҒm2пјҢеҲҷпјҡ
Cu+2Fe3+=Cu2++2Fe2+В В В В В В Fe+2Fe3+=3Fe2+
64gВ В 2molВ В В В В В В В В В В В В В В В В В 56gВ В В 2mol
m1В В В В 0.5molВ В В В В В В В В В В В В В В В m2В В В В 0.5mol
m1В =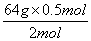 =16gпјҢ
=16gпјҢ
m2= =14gпјҢ
=14gпјҢ
жә¶и§Јзҡ„йҮ‘еұһиҙЁйҮҸдёәпјҡ18g-2.8g=15.2gпјҢ14g<15.2g<16gпјҢ
еҲҷй“Ғе®Ңе…ЁеҸҚеә”гҖҒй“ңйғЁеҲҶеҸҚеә”пјҢдё”Fe3+е®Ңе…ЁеҸҚеә”пјҢеү©дҪҷзҡ„йҮ‘еұһдёәCuпјҢж•…AгҖҒCй”ҷиҜҜпјӣ
и®ҫеҸҚеә”ж¶ҲиҖ—й“ңзҡ„зү©иҙЁзҡ„йҮҸдёәn1пјҢеҸҚеә”зҡ„й“Ғзҡ„зү©иҙЁзҡ„йҮҸдёәn2пјҢ
еҲҷпјҡ(1)64 n1+56 n2=15.2g
(2)n1+n2=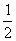 n(Fe3+)=0.25molпјҢ
n(Fe3+)=0.25molпјҢ
и®Ўз®—еҫ—еҮәпјҡn1=0.15molгҖҒn2=0.1molпјҢ
еҲҷеҺҹжқҘж··еҗҲзү©дёӯеҗ«жңүзҡ„й“ңзҡ„иҙЁйҮҸдёәпјҡ0.15molГ—64g/mol+2.8g=12.4gпјҢж•…Bй”ҷиҜҜпјӣ
ж №жҚ®иҙЁйҮҸе®ҲжҒ’е®ҡеҫӢпјҢжә¶ж¶Ідёӯдәҡй“ҒзҰ»еӯҗе’Ңй“ңзҰ»еӯҗзҡ„зү©иҙЁзҡ„йҮҸдёәпјҡn(Fe2+)+n(Cu2+)=0.15mol+0.10mol+0.5mol=0.75molпјҢжүҖд»ҘDйҖүйЎ№жҳҜжӯЈзЎ®зҡ„гҖӮ
зӯ”жЎҲйҖүDгҖӮ
