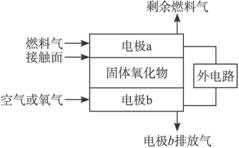
A.电极b为电池负极,电极反应式为O2+4e-====4O2-
B.固体氧化物的作用是让电子在电池内通过
C.若H2作为燃料气,则接触面上发生的反应为H2+2OH--4e-====2H++H2O
D.若C2H4作为燃料气,则接触面上发生的反应为C2H4+6O2--12e-====2CO2+2H2O

A.电极b为电池负极,电极反应式为O2+4e-====4O2-
B.固体氧化物的作用是让电子在电池内通过
C.若H2作为燃料气,则接触面上发生的反应为H2+2OH--4e-====2H++H2O
D.若C2H4作为燃料气,则接触面上发生的反应为C2H4+6O2--12e-====2CO2+2H2O
D
解析:本题主要考查了原电池的工作原理和燃料电池的有关知识。根据原电池工作原理,电子流出的一极是负极,流入的一极是正极。在此电池中燃料气发生氧化反应,失电子,电子流出是负极;氧气发生还原反应,得电子,电子流入是正极,故a为负极,b为正极,A错。在电池内部是电解质中离子定向移动导电,B错误。C选项中电解质是固体氧化物中无OH-,所以正确写法是:H2+O2-+2e-====H2O,C错。