用18 mol/L 的浓硫酸配制100 ml 3.0 mol/L 稀硫酸的实验步骤如下: ① 计
用18 mol/L 的浓硫酸配制100 ml 3.0 mol/L 稀硫酸的实验步骤如下:
① 计算所用浓硫酸的体积 ② 量取一定体积的浓硫酸 ③ 稀释
④检漏、 转移、洗涤 ⑤定容、摇匀
回答下列问题:
(1)所需浓硫酸的体积是 (保留一位小数),量取浓硫酸所用的量筒的规格是 (用下列编号填空)。
A.10ml B.25ml C.50ml D.100ml
(2)上述步骤中第③步的具体操作是
(3)下列情况对所配制的稀硫酸浓度有何影响?(用偏大、偏小、无影响填写)
①取浓硫酸后,洗涤量筒,洗涤液一并转移到烧杯中 ;
②烧杯中的溶液未冷却就转移到容量瓶中 ;
③量取浓硫酸时,俯视刻度线 。
【答案】
(1)16.7mL;B;
(2)将浓硫酸转移到烧杯中,缓慢加入蒸馏水,并用玻璃棒搅拌。
(3)偏大;偏大;偏小

(3)①取浓硫酸后,洗涤量筒,洗涤液一并转移到烧杯中,导致量取的浓硫酸中硫酸物质的量偏大,溶液浓度偏大,故答案为:偏大;
②烧杯中的溶液未冷却就转移到容量瓶中,导致溶液体积偏小,溶液浓度偏大,故答案为:偏大。
③量取浓硫酸时,俯视刻度线,导致溶质的物质的量偏小,溶液浓度偏小,故答案为:偏小。
【考点定位】考查配制一定物质的量浓度的溶液
【名师点晴】本题考查了配制一定物质的量浓度的溶液中的方法。配制一定物质的量浓度的溶液步骤有:计算、称量、溶解、冷却转移、洗涤转移、定容、摇匀。配制一定物质的量浓度溶液的常见误差分析的基本方法:紧抓c=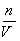 分析:如①用量筒量取浓硫酸倒入小烧杯后,用蒸馏水洗涤量筒并将洗涤液转移至小烧杯中,会造成结果偏大,因为量筒中的残留液是量筒的自然残留液,在制造仪器时已经将该部分的体积扣除,若洗涤并将洗涤液转移到容量瓶中,所配溶液浓度偏高;②配制氢氧化钠溶液时,将称量好的氢氧化钠固体放入小烧杯中溶解,未冷却立即转移到容量瓶中并定容,会造成结偏大;因为氢氧化钠固体溶于水放热,定容后冷却至室温,溶液体积缩小,低于刻度线,浓度偏大,若是溶解过程中吸热的物质,则溶液浓度偏小等等。
分析:如①用量筒量取浓硫酸倒入小烧杯后,用蒸馏水洗涤量筒并将洗涤液转移至小烧杯中,会造成结果偏大,因为量筒中的残留液是量筒的自然残留液,在制造仪器时已经将该部分的体积扣除,若洗涤并将洗涤液转移到容量瓶中,所配溶液浓度偏高;②配制氢氧化钠溶液时,将称量好的氢氧化钠固体放入小烧杯中溶解,未冷却立即转移到容量瓶中并定容,会造成结偏大;因为氢氧化钠固体溶于水放热,定容后冷却至室温,溶液体积缩小,低于刻度线,浓度偏大,若是溶解过程中吸热的物质,则溶液浓度偏小等等。

