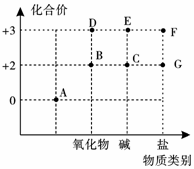
从化合价和物质类别两个维度认识元素及其化合物性质是重要的化学学
习方式。如图是Fe及其化合物的化合价--物质类别二维图。
【知识卡片】:
在化学反应中有元素化合价升高,则必有元素化合价降低,且化合价升高的总数一定等于化合价降低的总数。
请回答下列问题:
(1)A物质所属物质类别是______。
(2)D的化学式是______。
(3)可以用______(写化学式)和D在高温下反应生成A。
(4)G可以是硫酸盐,这种硫酸盐可用作贫血病人的补血剂,写出可生成该硫酸盐的化学方程式______(只写一个)。
(5)C在潮湿的空气中很容易发生化合反应变成E,该反应的化学方程式是______。
单质 Fe2O3 CO Fe+H2SO4=FeSO4+H2↑ 4Fe(OH)2+O2+2H2O=4Fe(OH)3
【解析】
解:(1)在A物质中化合价为0,所以A物质是单质;
(2)在D物质中铁显+3价,氧显-2价,化学式为:Fe2O3;
(3)可以用CO和Fe2O3在高温的条件下反应生成二氧化碳和铁;
(4)根据题意可知,G可以是硫酸亚铁,可以用铁和稀硫酸反应制取,化学方程式为:Fe+H2SO4=FeSO4+H2↑;
(5)根据题干提供信息可知,氢氧化亚铁和水、氧气反应生成氢氧化铁,化学方程式为:4Fe(OH)2+O2+2H2O═4Fe(OH)3。
故答案为:
(1)单质;
(2)Fe2O3;
(3)CO;
(4)Fe+H2SO4=FeSO4+H2;
(5)4Fe(OH)2+O2+2H2O═4Fe(OH)3。