为确定某铝热剂(含氧化铁和铝)的组成,分别进行下列实验:
(1)取a g样品,向其中加入足量的NaOH溶液,测得生成气体的体积为b L(标准状况,下同)。样品中铝的质量是_______g。(2)取a g样品,在高温条件下恰好完全反应,该反应的化学方程式是__________,氧化铁与铝的质量之比为____________。
(3)待(2)中的反应产物冷却后,加入足量盐酸,测得生成气体的体积为c L,该气体与(1)中所得气体的体积比c∶b=_____________。
(1)样品中加入NaOH溶液发生的反应的化学方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑。
由题意得: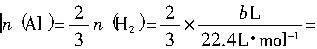
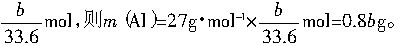
(2)样品在高温条件下发生铝热反应,反应的化学方程式为2Al+Fe2O3 2Fe+Al2O3,因为恰好完全反应,所以n(Fe2O3)∶n(Al)=1∶2,则m(Fe2O3)∶m(Al)=80∶27。
2Fe+Al2O3,因为恰好完全反应,所以n(Fe2O3)∶n(Al)=1∶2,则m(Fe2O3)∶m(Al)=80∶27。
(3)因为两份样品均为a g,由(1)、(2)得样品中的Al与生成的Fe的物质的量之比为1∶1。根据反应的化学方程式:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,2Al+Fe2O3 2Fe+Al2O3,Fe+2HCl=FeCl2+H2↑,可得c∶b=2∶3。
2Fe+Al2O3,Fe+2HCl=FeCl2+H2↑,可得c∶b=2∶3。