25、在某一容积为2L的密闭容器内,加入0.8mol的H2和0.6mol的I2,在一定
25、在某一容积为2L的密闭容器内,加入0.8mol的H2和0.6mol的I2,在一定的条件下发生如下反应:
H2(g) + I2(g) 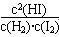 2HI(g) + Q (Q>0)
2HI(g) + Q (Q>0)
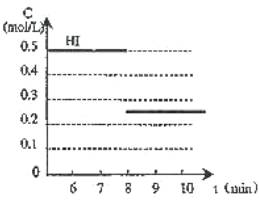
反应中各物质的浓度随时间变化情况如图1:
(1)该反应的化学平衡常数表达式为 。
(2)根据图1数据,反应开始至达到平衡时,平均速率v(HI)为 。
(3)反应达到平衡后,第8分钟时:
①若升高温度,化学平衡常数K (填写增大、减小或不变)
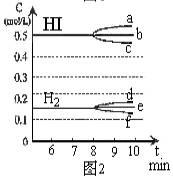
HI浓度的变化正确的是 (用图2中a-c的编号回答)
②若加入I2,H2浓度的变化正确的是 ,(用图2中d-f的编号回答)
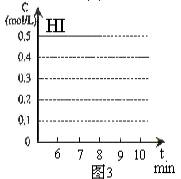
(4)反应达到平衡后,第8分钟时,若把容器的容积扩大一倍,请在图3中画出8分钟后HI浓度的变化情况
答案:
(1)K = 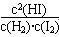
(2)0.167mol/L·min
(3)① 减小 c ② f
(4)见图

解析:本题综合考查化学反应速率、化学平衡、化学平衡常数及其影响因素等内容。
(1)由化学平衡常数的概念可知所给反应的化学平衡常数表达式为:K= 。
。
(2)由图1可知在3 min时反应达到平衡状态,HI的浓度变化为0.5 mol·L-1,
所以v(HI)= 0.5 mol·L-1/3 min=0.167 mol·L-1·min-1。
(3)①由于反应放热,温度升高,平衡向左移动,故K值减小,c(HI)减小即为图2中的c曲线;②若加入I2则c(I2)增大,平衡向右移动,c(H2)降低,d、e、f曲线中只有f适合。
(4)由于该反应为气体总体积不变的反应,所以在温度不变时,体积增大一倍,平衡不移动,但每种物质的浓度都变为原来的1/2。
![]() 2HI(g) + Q (Q>0)
2HI(g) + Q (Q>0)


