将Na2O2和NaHCO3的混合物加热(温度大于120℃),试分析可能发生反
将Na2O2和NaHCO3的混合物加热(温度大于120℃),试分析可能发生反应的化学方程式及最后产生气体和残余固体的成分。
当Na2O2不足时,发生反应①、②,残留固体为Na2CO3,生成的气体为CO2、O2、H2O;当Na2O2恰好与CO2反应完全时,发生反应①、②,残留固体为Na2CO3,生成气体为O2、H2O;当Na2O2还能与H2O(H2O过量)反应时,发生反应①、②、③,残留固体为Na2CO3、NaOH,生成气体为O2、H2O;当Na2O2还能恰好与H2O反应完全时,发生反应①、②、③,残留固体为Na2CO3、NaOH,生成气体为O2;当Na2O2过量时,残留固体为Na2CO3、NaOH、Na2O2,最后气体为O2。【试题分析】解析:若想直接写出Na2O2和NaHCO3反应的总反应方程式,再判断残余固体及最后产生气体的成分是不易实现的。可以将总反应过程认为是通过以下三个过程或阶段完成的:①NaHCO3受热分解:2NaHCO3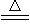 Na2CO3+CO2↑+H2O,②Na2O2先与CO2反应:2Na2O2+2CO2=2Na2CO3+O2,③Na2O2再与H2O反应:2Na2O2+2H2O=4NaOH+O2↑。这样,困难问题就转化为基础性知识的应用了。
Na2CO3+CO2↑+H2O,②Na2O2先与CO2反应:2Na2O2+2CO2=2Na2CO3+O2,③Na2O2再与H2O反应:2Na2O2+2H2O=4NaOH+O2↑。这样,困难问题就转化为基础性知识的应用了。