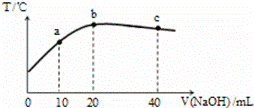
向20 mL 0.5 mol/L的氨水中逐滴加入等物质的量浓度的盐酸,测定溶液的温度变化如图所示。下列关于混合溶液的说法错误的是
A.从a点到b点,混合溶液不可能存在:c(Cl-)=c(NH4+)
B.由水电离的c(H+):b点>c点
C.氨水的电离平衡常数:b点>a点
D.b焦到c点,混合溶液中可能存在:c(Cl一)>c(H十) >c(NH4+)>c(OH-)
向20 mL 0.5 mol/L的氨水中逐滴加入等物质的量浓度的盐酸,测定溶液的温度变化如图所示。下列关于混合溶液的说法错误的是

A.从a点到b点,混合溶液不可能存在:c(Cl-)=c(NH4+)
B.由水电离的c(H+):b点>c点
C.氨水的电离平衡常数:b点>a点
D.b焦到c点,混合溶液中可能存在:c(Cl一)>c(H十) >c(NH4+)>c(OH-)
【答案】A
【解析】
试题分析:A、如果c(Cl-)=c(NH4+),根据电荷守恒知,溶液中c(OH-)=c(H+),氯化铵是强酸弱碱盐,其水溶液呈酸性,要使其溶液呈中性,则氨水应该稍微过量,所以从a点到b点,混合溶液中可能存在:c(Cl-)=c(NH4+),故A错误;B、b点酸碱恰好反应生成氯化铵,c点盐酸过量,盐酸抑制水电离,氯化铵促进水电离,所以由水电离出的c(H+):b点>c点,故B正确;C、氨水是弱电解质,在水溶液里存在电离平衡,且其电离过程吸热,温度越高,氨水的电离程度越大,其电离常数越大,故C正确;D、从b点到c点,盐酸过量,溶液中的溶质是氯化铵和盐酸,当盐酸的物质的量大于氯化铵的物质的量时,混合溶液中存在:c(Cl-)>c(H+)>c(NH4+)>c(OH-),故D正确,故选A。
考点:考查酸碱混合溶液定性判断