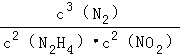阱(N 2H4)常用于火箭或原电池的燃料.己知:
①N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ/mol
②N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=﹣534.0kJ•mol
③H2O(g)=H2O(1)△H=﹣44kJ/mol
(1)2N2H4(g)+2NO2(g)=3N2(g)+4H2O(1)△H= kJ.mol﹣1
(2)一定温度下,将N2H4与N02以体积比1:1置于10L密闭容器中发生反应:2N2H4(g)+2NO2(g)=3N2(g)+4H2O(1)
下列不能说明反应达到平衡状态的是 .(填序号)
a.混合气体密度保持不变 b.混合气体颜色保持不变
c.N2H4比与NO2体积比保持不变 d.体系压强保持不变
(3)在10L的密闭容器中发生上述反应,容器内部分物质的物质的量变化如下表:
| 物质的量/时间 | n(N2H4) | n(NO2) | n(N2) |
| 起始 | 0.8 | 1.6 | 0 |
| 第2min | 0.6 | a | 0.3 |
| 第5min | 0.4 | 1.2 | 0.6 |
| 第6min | 0.4 | 1.2 | 0.6 |
| 第10min | 0.6 | 1.4 | 0.3 |
前2min内NO2的平均反应速率为 .平衡时N02的转化率 (2)中反应平衡常数表达式为 K= ,计算该温度下反应的平衡常数K= .反应在第6min时改变了条件,改变的条件可能是 (填序号)a.使用催化剂b.升高温度c.扩大容器容积d.增加N02的量
(4)若在一定温度下,(2)中反应的平衡常数为20,反应到某时刻测得N2H4、NO2、N2的溶度均为0.1mol.L﹣1,此时v正 v逆.
【考点】热化学方程式;化学平衡的影响因素;化学平衡状态的判断;化学平衡的计算.
【专题】化学反应中的能量变化;化学平衡专题.
【分析】(1)已知:①N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ/mol
②N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=﹣534.0kJ•mol
③H2O(g)=H2O(1)△H=﹣44kJ/mol
②×2﹣①+③×4得到:2N2H4(g)+2NO2(g)=3N2(g)+4H2O(1)根据盖斯定律计算反应的焓变;
(2)根据化学平衡的特征“等”、“定”及由此衍生的一些量来判断平衡;
(3)根据v=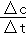 计算反应速率,根据转化率等于变化量和初始量的比值来计算;平衡常数K=
计算反应速率,根据转化率等于变化量和初始量的比值来计算;平衡常数K= ,根据影响化学反应速率和平衡移动的因素来回答;
,根据影响化学反应速率和平衡移动的因素来回答;
(4)根据Qc可K的关系确定反应的移动方向,进而确定正逆反应速率的大小.
【解答】解:(1)已知:①N2(g)+2O2(g)=2NO2(g)△H=+67.7kJ/mol
②N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=﹣534.0kJ•mol
③H2O(g)=H2O(1)△H=﹣44kJ/mol
②×2﹣①+③×4得到:2N2H4(g)+2NO2(g)=3N2(g)+4H2O(1)根据盖斯定律,△H=2×(﹣534.0kJ/mol)﹣67.7kJ/mol+4×(﹣44kJ/mol)=﹣1311.7kJ/mol;
故答案为:﹣1311.7;
(2)a.混合气体密度等于质量和体积的比值,但是密度始终保持不变,所以不一定是平衡状态,故错误;
b.混合气体颜色保持不变,说明各组分的浓度不随着时间的改变而改变,达到了平衡,故正确;
c.将N2H4与N02以体积比1:1置于密闭容器中,N2H4比与NO2体积比始终保持不变,此时不一定是平衡状态,故错误;
d.反应前后气体的系数和不变化,所以体系压强保持不变,说明反应达到了平衡,故正确;
故选ac;
(3)前2min内NO2的平均反应速率为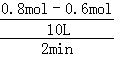 =0.01mol/(L•min),平衡时N02的转化率
=0.01mol/(L•min),平衡时N02的转化率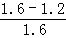 ×100%=25%,(2)中反应平衡常数表达式为K=
×100%=25%,(2)中反应平衡常数表达式为K=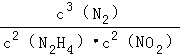 ,计算该温度下反应的平衡常数K=
,计算该温度下反应的平衡常数K=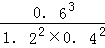 =0.9375,反应在第6min时改变了条件,此时各组分的浓度仍然保持不变,但是到了10min时,反应物的浓度增加,产物浓度减小,所以改变的条件可能是升高温度或是扩大容器容积,平衡逆向移动的结果,故选bc;故答案为:0.01mol/(L•min);25%;K=
=0.9375,反应在第6min时改变了条件,此时各组分的浓度仍然保持不变,但是到了10min时,反应物的浓度增加,产物浓度减小,所以改变的条件可能是升高温度或是扩大容器容积,平衡逆向移动的结果,故选bc;故答案为:0.01mol/(L•min);25%;K=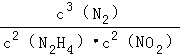 ;0.9375;bc;
;0.9375;bc;
(4)若在一定温度下,(2)中反应的平衡常数为20,反应到某时刻测得N2H4、NO2、N2的溶度均为0.1mol.L﹣1,此时Qc=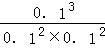 =10<K,所以v正>v逆,故答案为:>.
=10<K,所以v正>v逆,故答案为:>.
【点评】本题考查学生盖斯定律的应用、反应速率的计算以及化学平衡的有关计算等知识,属于综合知识的考查,难度中等.