使用氯化钠作原料可以得到多种产品。 (1)实验室用惰性电极电解100 m
使用氯化钠作原料可以得到多种产品。
(1)实验室用惰性电极电解100 mL 0.1 mol·L-1 NaCl溶液,若阴阳两极均得到112 mL气体(标准状况),则所得溶液的物质的量浓度是______________(忽略反应前后溶液体积的变化)。
(2)某学生想制作一种家用环保型消毒液发生器,用石墨作电极电解饱和氯化钠溶液,通电时,为使Cl2被完全吸收,制得有较强杀菌能力的消毒液,设计了如图的装置。

对电源电极名称和消毒液的主要成分判断正确的是________(填字母序号)。
A.a为正极,b为负极;NaClO和NaCl
B.a为负极,b为正极;NaClO和NaCl
C.a为阳极,b为阴极;HClO和NaCl
D.a为阴极,b为阳极;HClO和NaCl
(3)实验室中很难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀。某同学利用上图装置,只更换一个电极,通过电解法制取较纯净的Fe(OH)2沉淀,且较长时间不变色。该同学换上的电解材料是__________(用元素符号表示),总的反应式是___________。
答案 (1)0.1 mol·L-1 (2)B
(3)Fe Fe+2H2O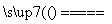 Fe(OH)2↓+H2↑
Fe(OH)2↓+H2↑
解析 (1)n(H2)=n(Cl2)=0.005 mol,参加反应的n(NaCl)=0.01 mol,说明NaCl恰好电解完毕,溶液变为NaOH溶液,n(NaOH)=n(NaCl)=0.01 mol,c(NaOH)=0.1 mol·L-1。
(2)电解饱和氯化钠溶液的总反应:2NaCl+2H2O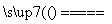 2NaOH+H2↑+Cl2↑,题目要求使Cl2被完全吸收,则氯气必须在下部的电极上产生,下部的电极是阳极,推出b为电源的正极,另一极为负极a。生成的Cl2与阴极区产生的NaOH反应:Cl2+2NaOH===NaCl+NaClO+H2O,则消毒液的主要成分是NaClO、NaCl。
2NaOH+H2↑+Cl2↑,题目要求使Cl2被完全吸收,则氯气必须在下部的电极上产生,下部的电极是阳极,推出b为电源的正极,另一极为负极a。生成的Cl2与阴极区产生的NaOH反应:Cl2+2NaOH===NaCl+NaClO+H2O,则消毒液的主要成分是NaClO、NaCl。
(3)题目要求通过电解法制取Fe(OH)2,电解质溶液是NaCl溶液,必须通过电极反应产生Fe2+和OH-。根据电极发生反应的特点,选择铁作阳极,铁发生氧化反应产生Fe2+;溶液中的阳离子Na+、H+向阴极移动,根据放电顺序,阴极H+放电产生氢气,H+来源水的电离,反应式2H2O+2e-===H2↑+2OH-。在电场作用下,阳极产生的Fe2+与阴极产生的OH-在定向移动的过程中相遇,发生复分解反应生成Fe(OH)2沉淀。将阳极反应式、阴极反应式叠加得到总的反应式:Fe+2H2O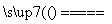 Fe(OH)2↓+H2↑。
Fe(OH)2↓+H2↑。
题组二 电解原理的“不寻常”应用

