(1)已知反应A+3B2C+D,在30 s内A的浓度减小了0.5 mol·L-1,则此段时间内以B
(1)已知反应A+3B 2C+D,在30 s内A的浓度减小了0.5 mol·L-1,则此段时间内以B的浓度变化表示的反应速率为
2C+D,在30 s内A的浓度减小了0.5 mol·L-1,则此段时间内以B的浓度变化表示的反应速率为
mol·L-1·min-1,以C的浓度变化表示的反应速率为 mol·L-1·min-1。
(2)在恒温恒容条件下,反应2SO2+O2 2SO3进行一段时间后,SO3的浓度增加了0.4 mol·L-1,在这段时间内用O2表示的反应速率为0.04 mol·L-1·s-1,则这段时间为 s。
2SO3进行一段时间后,SO3的浓度增加了0.4 mol·L-1,在这段时间内用O2表示的反应速率为0.04 mol·L-1·s-1,则这段时间为 s。
(3)将物质的量相等的A、B混合于2 L密闭容器中,发生如下反应:3A(g)+B(g)
 xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol·L-1,c(A)∶c(B)=3∶5,
xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol·L-1,c(A)∶c(B)=3∶5,
C的平均反应速率是0.1 mol·L-1·min-1。回答下列问题:
①x值是 。
②用B表示的5 min内的平均反应速率为_______________________________。
③反应开始前放入容器中的A、B物质的量各为 。
【解析】(1)由题意可知用A表示的反应速率为1 mol·L-1·min-1,根据化学计量数之比可求出以B的浓度变化表示的反应速率为3 mol·L-1·min-1,以C的浓度变化表示的反应速率为2 mol·L-1·min-1。
(2)该段时间内,SO3的浓度增加了0.4 mol·L-1,根据方程式O2的浓度减小了
0.2 mol·L-1,那么,Δt=Δc(O2)/v(O2)=5 s。
(3)D的起始浓度为0,浓度变化量为0.5 mol·L-1,则v(D)=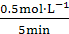 =
=
0.1 mol·L-1·min-1,由v(C)∶v(D)=x∶2=0.1 mol·L-1·min-1∶0.1 mol·L-1·min-1=
1∶1,得x=2。v(B)= v(D)=0.05 mol·L-1·min-1。设反应开始时加入的A、B的物质的量均为n,反应过程中生成1 mol D,则消耗1.5 mol A、0.5 mol B,则有:
v(D)=0.05 mol·L-1·min-1。设反应开始时加入的A、B的物质的量均为n,反应过程中生成1 mol D,则消耗1.5 mol A、0.5 mol B,则有:
3A(g) + B(g) xC(g)+2D(g)
xC(g)+2D(g)
起始量 n n
变化量 1.5 mol 0.5 mol
终点量 n-1.5 mol n-0.5 mol
容器体积相同,物质的量之比=浓度之比,因此可建立关系式: =
= ,
,
得n=3 mol。
答案:(1)3 2 (2)5
(3)①2 ②0.05 mol·L-1·min-1 ③3 mol、3 mol
![]() 2C+D,在30 s内A的浓度减小了0.5 mol·L-1,则此段时间内以B的浓度变化表示的反应速率为
2C+D,在30 s内A的浓度减小了0.5 mol·L-1,则此段时间内以B的浓度变化表示的反应速率为 ![]() 2SO3进行一段时间后,SO3的浓度增加了0.4 mol·L-1,在这段时间内用O2表示的反应速率为0.04 mol·L-1·s-1,则这段时间为 s。
2SO3进行一段时间后,SO3的浓度增加了0.4 mol·L-1,在这段时间内用O2表示的反应速率为0.04 mol·L-1·s-1,则这段时间为 s。![]() xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol·L-1,c(A)∶c(B)=3∶5,
xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol·L-1,c(A)∶c(B)=3∶5,