现有工厂丢弃的废铜屑(铜屑表面呈绿色,其中混有少量生锈铁屑)。课
现有工厂丢弃的废铜 屑(铜屑表面呈绿色,其中混有少量生锈铁屑)。课外活动小组同学欲利用其制
屑(铜屑表面呈绿色,其中混有少量生锈铁屑)。课外活动小组同学欲利用其制
 取胆矾,他们设计了下面的两种制取流程。
取胆矾,他们设计了下面的两种制取流程。
已知Cu+Fe2(SO4)3 2FeSO4+CuSO4,请回答:
2FeSO4+CuSO4,请回答:
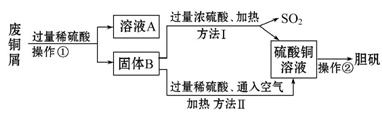
(1) 铜屑表面呈绿色的物质化学式是Cu2(OH)2CO3,俗称 ,操作①所用到的玻璃仪器有烧杯、玻璃棒和 。
铜屑表面呈绿色的物质化学式是Cu2(OH)2CO3,俗称 ,操作①所用到的玻璃仪器有烧杯、玻璃棒和 。
(2)溶液A的溶质有 (只写一种);铁锈与稀硫酸反应的化学方程式为 。
(3)两种方法比较,符合绿色化学要求的是方法 ;方法Ⅱ的化学方程式为2Cu+2H2SO4+  2CuSO4+ ,操作②实验步骤为 ,降温结晶。
2CuSO4+ ,操作②实验步骤为 ,降温结晶。
【解析】(1)铜屑表面呈绿色的物质为碱式碳酸铜,其俗称为铜绿;操作①是将固体、液体分离,属于过滤操作,用到的玻璃仪器为烧杯、玻璃棒和漏斗。(2)废铜屑中含有铜、铜绿、铁、铁锈、不溶性杂质,加入稀硫酸后能发生的反应有
①Cu2(OH)2CO3+2H2SO4 2CuSO4+3H2O+CO2↑,②Fe2O3+3H2SO4
2CuSO4+3H2O+CO2↑,②Fe2O3+3H2SO4 Fe2(SO4)3+3H2O,
Fe2(SO4)3+3H2O,
③Cu+Fe2(SO4)3 2FeSO4+CuSO4,④Fe+H2SO4
2FeSO4+CuSO4,④Fe+H2SO4 FeSO4+H2↑,
FeSO4+H2↑, 可以判断溶质中一定有FeSO4、CuSO4、H2SO4,固体B中一定含有Cu。(3)方法Ⅰ产生SO2会对空气造成污染,所以方法Ⅱ更符合绿色化学的要求;操作②是从硫酸铜溶液中制取胆矾,要蒸发溶剂。
可以判断溶质中一定有FeSO4、CuSO4、H2SO4,固体B中一定含有Cu。(3)方法Ⅰ产生SO2会对空气造成污染,所以方法Ⅱ更符合绿色化学的要求;操作②是从硫酸铜溶液中制取胆矾,要蒸发溶剂。
答案:(1)铜绿 漏斗
(2)FeSO4、CuSO4、H2SO4(或硫酸铜、硫酸亚铁、硫酸)(任写一种即可)
Fe2O3+3H2SO4 Fe2(SO4)3+3H2O
Fe2(SO4)3+3H2O
(3)Ⅱ O2 2H2O 蒸发浓缩
![]() 屑(铜屑表面呈绿色,其中混有少量生锈铁屑)。课外活动小组同学欲利用其制
屑(铜屑表面呈绿色,其中混有少量生锈铁屑)。课外活动小组同学欲利用其制![]()
![]() 取胆矾,他们设计了下面的两种制取流程。
取胆矾,他们设计了下面的两种制取流程。![]() 2FeSO4+CuSO4,请回答:
2FeSO4+CuSO4,请回答:
![]() 铜屑表面呈绿色的物质化学式是Cu2(OH)2CO3,俗称 ,操作①所用到的玻璃仪器有烧杯、玻璃棒和 。
铜屑表面呈绿色的物质化学式是Cu2(OH)2CO3,俗称 ,操作①所用到的玻璃仪器有烧杯、玻璃棒和 。![]() 2CuSO4+ ,操作②实验步骤为 ,降温结晶。
2CuSO4+ ,操作②实验步骤为 ,降温结晶。