甲、乙两个实验小组分别进行“Na2CO3和NaCl混合物中Na2CO3含量的测定
甲、乙两个实验小组分别进行“Na
2CO
3和NaCl混合物中Na
2CO
3含量的测定”的实验:
(1)甲组用沉淀分析法,把一定量的混合物溶解后加入足量的CaCl2,然后过滤,他们在用过滤装置操作时,还要进行的一项操作是____________________________。在整个实验过程中,使用天平至少要_______次。
(2)乙组用气体分析法,把一定量的混合物与足量的盐酸反应后,然后用图2-1-3所示装置测定产生的CO2气体的体积,请分析广口瓶中的溶液是_______,该装置测定的气体体积是否准确,说明理由:__________________________________________。
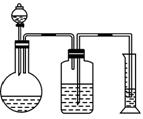
图2-1-3
(3)请你再设计一个与甲、乙组操作不同的实验方法,测定混合物中的Na2CO3含量。方法是____________________________。用到的主要试剂是_______ (至少两种),用到的仪器主要是_______________________________________________________________(至少两件)。
解析:(1)因为过滤所得到的固体表面上附有溶液中某些离子,需要加水将滤渣洗涤2—3次。要测定混合物中碳酸钠的含量,需知混合物的总质量及产生碳酸钙的质量,而碳酸钙质量的获得则要求干燥后两次称量的误差不大于0.1 g,故使用天平的次数至少要3次。
(2)由于二氧化碳溶于水且存在平衡:
CO2+H2O H2CO3
H2CO3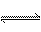 H++
H++ 为减少二氧化碳的溶解量,广口瓶中可加入饱和NaHCO3溶液。但由于反应产生的二氧化碳中混有少量的HCl气体,与NaHCO3反应产生二氧化碳,所以利用该装置测定的二氧化碳体积是不准确的。
为减少二氧化碳的溶解量,广口瓶中可加入饱和NaHCO3溶液。但由于反应产生的二氧化碳中混有少量的HCl气体,与NaHCO3反应产生二氧化碳,所以利用该装置测定的二氧化碳体积是不准确的。
(3)因为碳酸钠溶液与盐酸反应,而氯化钠与盐酸不反应,所以可用标准盐酸溶液滴定一定质量的混合物,根据消耗盐酸溶液的体积来测定碳酸钠的含量。
答案:(1)沉淀的洗涤 3次
(2)饱和NaHCO3溶液 不准确,少量HCl与NaHCO3反应产生了CO2
(3)中和分析法(或中和滴定法,或用标准盐酸溶液滴定一定量的混合物溶液) 标准准盐酸溶液、甲基橙 滴定管、锥形瓶

