下表是元素周期表的一部分,针对表中的a~g元素,回答下列问题:
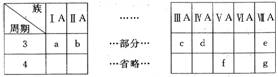
(1)d元素位于金属与非金属的分界线处,常用作 材料。
(2) f的元素符号为As,其最高价氧化物的化学式为 。
(3)a、b、c三种元素的最高价氧化物对应水化物的碱性逐渐减弱,试从原子结构的角度解释上述变化规律 。
(4)e元素的非金属性强于g,请写出一个离子方程式证明: 。
下表是元素周期表的一部分,针对表中的a~g元素,回答下列问题:

(1)d元素位于金属与非金属的分界线处,常用作 材料。
(2) f的元素符号为As,其最高价氧化物的化学式为 。
(3)a、b、c三种元素的最高价氧化物对应水化物的碱性逐渐减弱,试从原子结构的角度解释上述变化规律 。
(4)e元素的非金属性强于g,请写出一个离子方程式证明: 。
(1)半导体 (2)As2O5
(3)电子层数相同,核电荷数增加,原子半径减小,失电子能力减弱,金属性减弱。
(4)Cl2+2Br-=Br2+2Cl-