将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s)![]() 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示,已知Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,下列说法正确的是
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示,已知Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,下列说法正确的是
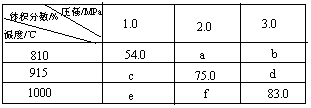
A.b>f
B.平衡常数K(1000℃)<K(810℃)
C.915℃,2.0MPa该反应的平衡常数为Kp=4.5MPa
D.1000℃,3.0MPa时E的转化率为83%
将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s)![]() 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示,已知Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,下列说法正确的是
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示,已知Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,下列说法正确的是

A.b>f
B.平衡常数K(1000℃)<K(810℃)
C.915℃,2.0MPa该反应的平衡常数为Kp=4.5MPa
D.1000℃,3.0MPa时E的转化率为83%
C
【解析】该反应为体积增大的反应,故加压时,平衡逆向移动,从表中第一行数据,54.0
>a>b;结合表中第3列数据,可确定75.0>a,故正反应为吸热反应,△H >0,依据变化条件,还可确定:e>c>54.0;c>75.0 >d ;e>f>83.0 ,故b<f,故A项和B项均不正确;C项:p(G)=2.0MPa×75%=1.5MPa,p(E)=2.0MPa×25%=0.5MPa,
Kp=![]()
D项:E(g) + F(s)![]() 2G(g),设起始时,E为a mol,转化x mol,由于F为固体,对平衡无影响。则平衡时:E为(a-x),G为2x,
2G(g),设起始时,E为a mol,转化x mol,由于F为固体,对平衡无影响。则平衡时:E为(a-x),G为2x,![]() ,得x≈0.709a,所以E的转化率为x/a ≈ 70.9%,D错误。
,得x≈0.709a,所以E的转化率为x/a ≈ 70.9%,D错误。