дёӢиЎЁдёәй•ҝејҸе‘ЁжңҹиЎЁзҡ„дёҖйғЁеҲҶпјҢе…¶дёӯзҡ„еәҸеҸ·д»ЈиЎЁеҜ№еә”зҡ„е…ғзҙ гҖӮ в‘ в‘Ўв‘ў
дёӢиЎЁдёәй•ҝејҸе‘ЁжңҹиЎЁзҡ„дёҖйғЁеҲҶпјҢе…¶дёӯзҡ„еәҸеҸ·д»ЈиЎЁеҜ№еә”зҡ„е…ғзҙ гҖӮ
| в‘ | | | | | | | | | | | | | | | | | гҖҖ |
| гҖҖ | в‘Ў | | | | | | | | | | | гҖҖ | в‘ў | в‘Ј | в‘Ө | в‘Ҙ | гҖҖ |
| гҖҖ | в‘Ұ | | | | | | | | | | гҖҖ | ⑧гҖҖ | гҖҖ | гҖҖ | гҖҖ | | гҖҖ |
| гҖҖ | гҖҖ | гҖҖ | гҖҖ | гҖҖ | в‘Ё | гҖҖ | гҖҖ | гҖҖ | гҖҖ | в‘© | гҖҖ | гҖҖ | гҖҖ | гҖҖ | гҖҖ | гҖҖ | гҖҖ |
пјҲ1пјүеҶҷеҮәдёҠиЎЁдёӯе…ғзҙ в‘Өзҡ„иҪЁйҒ“иЎЁзӨәејҸ_______пјҢе…ғзҙ в‘ЁеҺҹеӯҗзҡ„ж ёеӨ–з”өеӯҗжҺ’еёғејҸ__________гҖӮ
пјҲ2пјүе…ғзҙ 第дёҖз”өзҰ»иғҪзҡ„еӨ§е°ҸжҜ”иҫғпјҡв‘Ј_____в‘ӨпјҲеЎ«еҶҷвҖңпјһвҖқвҖңпјқвҖқжҲ–вҖңпјңвҖқпјҢдёӢеҗҢпјүпјӣе…ғзҙ з”өиҙҹжҖ§зҡ„еӨ§е°ҸжҜ”иҫғпјҡв‘Ј_____в‘ӨпјҲеЎ«еҶҷвҖңпјһвҖқвҖңпјқвҖқжҲ–вҖңпјңвҖқпјүпјӣиҜ·еҶҷеҮәдёҺе…ғзҙ в‘Јзҡ„еҚ•иҙЁдә’дёәзӯүз”өеӯҗдҪ“зҡ„дёҖз§Қеҫ®зІ’зҡ„еҢ–еӯҰејҸ_________гҖӮ
пјҲ3пјүеңЁжөӢе®ҡе…ғзҙ в‘ дёҺв‘ҘеҪўжҲҗеҢ–еҗҲзү©зҡ„зӣёеҜ№еҲҶеӯҗиҙЁйҮҸж—¶пјҢе®һйӘҢжөӢеҫ—зҡ„еҖјдёҖиҲ¬й«ҳдәҺзҗҶи®әеҖјзҡ„дё»иҰҒеҺҹеӣ жҳҜ__________гҖӮ
(4)дёҠиҝ°в‘ўдёҺв‘Је…ғзҙ з»„жҲҗзҡ„(CN)2еҢ–еҗҲзү©дёӯ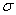 й”®дёҺ
й”®дёҺ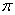 й”®д№ӢжҜ”________гҖӮ
й”®д№ӢжҜ”________гҖӮ
пјҲ5пјүв‘Ұзҡ„ж°§еҢ–зү©жҳҜдјҳиүҜзҡ„иҖҗй«ҳжё©жқҗж–ҷпјҢе®ғзҡ„зҶ”зӮ№жҜ” CaOй«ҳпјҢе…¶еҺҹеӣ жҳҜ_____________гҖӮ
пјҲ6пјүе…ғзҙ в‘©зҡ„жҹҗз§Қж°§еҢ–зү©зҡ„жҷ¶дҪ“з»“жһ„еҰӮеӣҫжүҖзӨәпјҢе…¶дёӯе®һеҝғзҗғиЎЁзӨәе…ғзҙ в‘©еҺҹеӯҗпјҢеҲҷиҜҘж°§еҢ–зү©зҡ„еҢ–еӯҰејҸ________гҖӮ

гҖҗзҹҘиҜҶзӮ№гҖ‘е…ғзҙ е‘ЁжңҹиЎЁгҖҒз”өзҰ»иғҪгҖҒз”өиҙҹжҖ§гҖҒеҢ–еӯҰй”®гҖҒжҷ¶дҪ“з»“жһ„
гҖҗзӯ”жЎҲи§ЈжһҗгҖ‘
В (1)гҖҒ
|
| 1SВ В В В В В 2SВ В В В В В В В В В В В 2p | В |
В пјҲ2еҲҶпјү
В [Ar]3d54s1В пјҲ2еҲҶпјү
В (2)В пјһВ пјӣВ <В пјӣВ В CO жҲ–C22- пјҲеҗ„1еҲҶпјү
(3)HFеҲҶеӯҗй—ҙд»Ҙж°ўй”®еҪўжҲҗиҒҡеҗҲ(HF)nеҲҶеӯҗпјҲ1еҲҶпјү
пјҲ4пјү3:4В В пјҲ2еҲҶпјү
пјҲ5пјүMg2+жҜ”Ca2+еҚҠеҫ„е°ҸпјҢзҰ»еӯҗй”®ејәпјҢMgOжҜ”CaOзҡ„жҷ¶ж јиғҪеӨ§пјҲ2еҲҶпјү
пјҲ6пјү Cu2O пјҲ2еҲҶпјү
В и§ЈжһҗпјҡпјҲ1пјүиЎЁдёӯе…ғзҙ в‘ӨжҳҜFе…ғзҙ пјҢз”өеӯҗжҺ’еёғејҸдёә1S22S22P5,жүҖд»ҘиҪЁйҒ“жҺ’еёғпјҡ
1SВ В В В В В 2SВ В В В В В В В В В В В 2p | В |
пјҲ2еҲҶпјү
В В В в‘ЁжҳҜ24еҸ·е…ғзҙ CrпјҢеҺҹеӯҗзҡ„ж ёеӨ–з”өеӯҗжҺ’еёғејҸ[Ar]3d54s1пјӣ
пјҲ2пјүеҗҢдёҖе‘Ёжңҹе…ғзҙ зҡ„第дёҖз”өзҰ»иғҪеҹәжң¬дёҠйҡҸеҺҹеӯҗеәҸж•°зҡ„йҖ’еўһиҖҢеўһеӨ§пјҢеҗҢдёҖдё»ж—Ҹе…ғзҙ зҡ„д»ҺдёҠеҲ°дёӢдёҖиҲ¬и¶ӢдәҺеҮҸе°ҸпјҢиҝҷдәӣйғҪе’Ңе…ғзҙ йҮ‘еұһжҖ§йҖ’еҸҳ规еҫӢдёҖиҮҙгҖӮеҮәзҺ°иҪЁйҒ“е…Ёе……ж»ЎгҖҒеҚҠе……ж»ЎзҠ¶жҖҒж—¶дҫӢеӨ–пјҢNе…ғзҙ 2pиғҪзә§е®№зәі3дёӘз”өеӯҗпјҢеӨ„дәҺеҚҠж»ЎзЁіе®ҡзҠ¶жҖҒпјҢиғҪйҮҸиҫғдҪҺпјҢеӨұеҺ»з¬¬дёҖдёӘз”өеӯҗйңҖиҰҒзҡ„иғҪйҮҸиҫғй«ҳпјҢ故第дёҖз”өзҰ»иғҪNпјһOе…ғзҙ пјӣе…ғзҙ з”өиҙҹжҖ§зҡ„еӨ§е°ҸдёҺйқһйҮ‘еұһжҖ§дёҖиҮҙпјӣе…ғзҙ в‘Јзҡ„еҚ•иҙЁжҳҜN2пјҢ14дёӘз”өеӯҗпјҢжңүCO жҲ–C22- зӯүпјӣпјҲ3пјүе…ғзҙ HдёҺFеҪўжҲҗеҢ–еҗҲзү©HFпјҢHFеҲҶеӯҗд№Ӣй—ҙеӯҳеңЁж°ўй”®пјҢеӯҳеңЁзј”еҗҲпјҲHFпјүnеҲҶеӯҗпјҢж•…е®һйӘҢжөӢеҫ—зҡ„зӣёеҜ№еҲҶеӯҗиҙЁйҮҸдёҖиҲ¬й«ҳдәҺзҗҶи®әеҖјпјӣпјҲ4пјү(CN)2зҡ„з»“жһ„ејҸжҳҜNвүЎC-CвүЎNпјҢеҚ•й”®йғҪжҳҜПғй”®пјӣеҸҢй”®дёҖдёӘжҳҜПғй”®пјҢдёҖдёӘжҳҜПҖй”®пјӣдёүй”®дёҖдёӘжҳҜПғй”®пјҢдёӨдёӘжҳҜПҖй”®гҖӮжүҖд»ҘПғй”®ж•°жҳҜ1+1+1=3пјҢПҖй”®ж•°жҳҜ2+2=4пјҢПҖй”®е’ҢПғй”®д№ӢжҜ”жҳҜ3:4пјӣпјҲ5пјүв‘Ұзҡ„ж°§еҢ–зү©жҳҜMgOпјҢMg2+жҜ”Ca2+еҚҠеҫ„е°ҸпјҢзҰ»еӯҗй”®ејәпјҢMgOжҜ”CaOзҡ„жҷ¶ж јиғҪеӨ§пјҢжүҖд»Ҙе®ғзҡ„зҶ”зӮ№жҜ” CaOй«ҳпјӣпјҲ6пјүж №жҚ®жҷ¶иғһзҡ„и®Ўз®—пјҡCuпјҡ4пјҢ Oпјҡ8Г—1/8+1=2пјҢж•…CuгҖҒOдёӘж•°жҜ”дёә2:1пјҢж•…еҢ–еӯҰејҸдёә Cu2O
гҖҗжҖқи·ҜзӮ№жӢЁгҖ‘жң¬йўҳиҖғжҹҘе…ғзҙ е‘ЁжңҹиЎЁгҖҒж ёеӨ–з”өеӯҗжҺ’еёғгҖҒз”өзҰ»иғҪгҖҒеҲҶеӯҗз»“жһ„дёҺжҖ§иҙЁзӯүпјҢйҡҫеәҰдёӯзӯүпјҢжіЁж„Ҹж°ўй”®еҜ№зү©иҙЁжҖ§иҙЁзҡ„еҪұе“ҚпјҢжҺҢжҸЎдёӯеӯҰеёёи§Ғжҷ¶иғһзҡ„и®Ўз®—гҖӮ
![]() й”®дёҺ
й”®дёҺ![]() й”®д№ӢжҜ”________гҖӮ
й”®д№ӢжҜ”________гҖӮ
