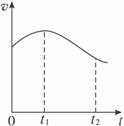

解析:影响镁和盐酸反应速率的因素主要有两个:浓度和温度。0~t1的速率由慢到快,显然从浓度这一因素考虑是不合适的,因为在整个反应过程中盐酸的浓度总是降低的,则使反应速率加快的原因只能是温度的升高,即推测该反应为放热反应,也就是该段时间内温度对反应速率的影响起了决定性的作用;但当浓度降到一定程度后,则浓度对反应速率的影响又占优势,起了决定性的作用,故t1之后化学反应速率变慢。
答案:该反应为放热反应,0~t1时间温度升高,对反应速率的影响占优势,使反应速率加快;t1以后,盐酸浓度降低对反应速率的影响占优势,使反应速率变慢