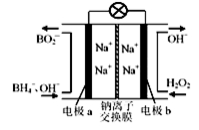
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2做原料的燃料电池,负极材料采用Pt/C.正极材料采用MnO2,可用做空军通信卫星电源,其工作原理如图所示。下列说法中不正确的是
A. 电池放电时Na+从a极区移向b极区
B. 燃料电池是一类能量转化效率高、环境友好的发电装置
C. 该电池的负极反应为BH4-+ 8OH-一8e-═BO2-+ 6H2O
D. 在电池反应中,每消耗3molH2O2,转移电子数为3NA
据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2做原料的燃料电池,负极材料采用Pt/C.正极材料采用MnO2,可用做空军通信卫星电源,其工作原理如图所示。下列说法中不正确的是

A. 电池放电时Na+从a极区移向b极区
B. 燃料电池是一类能量转化效率高、环境友好的发电装置
C. 该电池的负极反应为BH4-+ 8OH-一8e-═BO2-+ 6H2O
D. 在电池反应中,每消耗3molH2O2,转移电子数为3NA
D
【解析】由题意知,该燃料电池反应中,NaBH4作还原剂、H2O2作氧化剂。
A. 原电池工作时,阳离子一般向正极定向移动,所以电池放电时Na+从a极区移向b极区是正确的;B. 燃料电池是一类能量转化效率高、环境友好的发电装置,B是正确的;
C. 还原剂在负极发生氧化反应,由于负极同时通入了NaBH4和NaOH,所以该电池的负极反应为BH4-+ 8OH-一8e-═BO2-+ 6H2O,C正确;D. 在电池反应中,每消耗3molH2O2,O的化合价由-1降到-2价,所以转移电子数为6NA,D不正确。选D。
点睛:判断电极反应式是否正确时,可根据原电池原理,负极上发生氧化反应、正极发生还原反应,并用电解质溶液检验产物是否合理。