硬水受热后会产生水垢,水垢的主要成分是CaCO3和Mg(OH)2,其它成分不参与反应.实验室由水垢制取纯净CaCl2固体的流程如下:
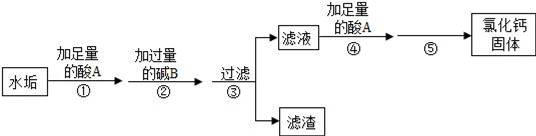

请按要求填空:
(1)酸A是人体胃酸的主要成分,酸A的化学式是 ;
(2)步骤②中生成沉淀的化学反应方程式是 ;
(3)步骤③中用到的玻璃仪器主要有烧杯、 、 ;
(4)步骤④加酸A的作用是 ;
(5)步骤⑤是利用 的方法得到氯化钙固体.
硬水受热后会产生水垢,水垢的主要成分是CaCO3和Mg(OH)2,其它成分不参与反应.实验室由水垢制取纯净CaCl2固体的流程如下:


请按要求填空:
(1)酸A是人体胃酸的主要成分,酸A的化学式是 ;
(2)步骤②中生成沉淀的化学反应方程式是 ;
(3)步骤③中用到的玻璃仪器主要有烧杯、 、 ;
(4)步骤④加酸A的作用是 ;
(5)步骤⑤是利用 的方法得到氯化钙固体.
【考点】物质的相互转化和制备;过滤的原理、方法及其应用;盐的化学性质;书写化学方程式、 .
【分析】(1)根据人体胃酸的主要成分是盐酸进行分析回答;
(2)根据氢氧化钙溶液和氯化镁反应生成氢氧化镁白色沉淀和氯化钙进行分析;
(3)根据过滤的操作分析用到的仪器;
(4)根据需要制取的是氯化钙和加入的过量碱B进行分析;
(5)根据结晶的方法分析回答.
【解答】解:(1)人体胃酸的主要成分是盐酸,所以酸A是盐酸,化学式为:HCl;
(2)碳酸钙和盐酸反应会生成氯化钙、水和二氧化碳、氢氧化镁和盐酸反应生成氯化镁和水,最后需要制取氯化钙,所以需要将氯化镁沉淀,依据除杂原则可知,B是氢氧化钙,所以步骤②中生成沉淀的反应是氯化镁和氢氧化钙反应生成氢氧化镁沉淀和氯化钙,化学方程式为:MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2;
(3)步骤③试将固液分开,操作是过滤,用到的玻璃仪器主要有烧杯、漏斗和玻璃棒
(4)前面加入的是过量的氢氧化钙,而最后要得到氯化钙,需要将氢氧化钙除去,所以步骤④加酸A的作用是:将反应剩余的氢氧化钙除去;
(5)滤液中加入盐酸反应后是盐酸和氯化钙的混合物,所以要从溶液中得到氯化钙,需要用蒸发结晶的方法.
故答案为:(1)HCl;(2)MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2;(3)漏斗,玻璃棒;(4)将反应剩余的氢氧化钙除去;(5)蒸发结晶.
【点评】本题难度不是很大,主要考查了酸的有关的化学性质及有关的化学方程式的书写,培养学生抓住规律、应用规律解决问题的能力.