二氧化氯(ClO2)是一种黄绿色有刺激性气味的气体,其熔点为-59oC
二氧化氯(ClO2)是一种黄绿色有刺激性气味的气体,其熔点为-59oC,沸点为11.0oC,易溶于水。是目前国际上公认的新一代高效、广谱、安全的杀菌、保鲜剂,在水处理等方面有广泛应用的高效安全消毒剂。与(Cl2)相比(ClO2)不但具有更显著的杀菌能力,而且不会产生对人体有潜在危害的有机氯代物。
(1)在ClO2的制备方法中,比较实用的有数十种,实验室常用氯酸钠(NaClO3)、亚硫酸钠(Na2SO3)和硫酸共热制备二氧化氯,此化学反应方程式为:
(2)工业上用稍潮湿的KClO3和草酸(H2C2O4)在60oC时反应制得。某学生用如图所示的装置模拟工业制取及收集ClO2,其中A为ClO2的发生装置,B为ClO2的凝集装置,C为尾气吸收装置。请问:
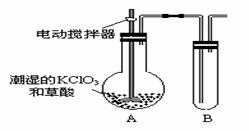
A部分还应添加温度控制装置,请你说出一种温度控制方法 ;
B部分还应补充什么装置___ _____________;
此实验装置还有何不足?
(3)我国最近成功研制出制取ClO2的新方法,其反应的微观过程如图所示:

该反应的化学方程式为 。
【答案】(1)2NaClO3+Na2SO3+H2SO4=2ClO2↑+2Na2SO4+H2O;
(2)水浴加热;(冰水)冷凝;缺少尾气处理装置;
(3)2NaClO2+Cl2=2NaCl+2ClO2
【解析】
试题分析:(1)用氯酸钠(NaClO3)、亚硫酸钠(Na2SO3)和硫酸共热制备二氧化氯,还生成硫酸钠和水,化学反应为2NaClO3+Na2SO3+H2SO4=2ClO2↑+2Na2SO4+H2O,故答案为:2NaClO3+Na2SO3+H2SO4=2ClO2↑+2Na2SO4+H2O;
(2)图1所示的装置模拟工业制取及收集ClO2,其中A为ClO2的发生装置,B为ClO2的凝集装置,C为尾气吸收装置,A应控制温度为60°C,温度控制方法为水浴加热;B应冷却分离,B部分还应补充冰水冷凝装置,该实验中尾气有毒,则实验装置的不足之处为缺少尾气处理装置,故答案为:水浴加热;(冰水)冷凝;缺少尾气处理装置;
(3)由微观过程可知,氯气与NaClO2反应,由原子及电子守恒可知,反应为2NaClO2+Cl2=2NaCl+2ClO2,故答案为:2NaClO2+Cl2=2NaCl+2ClO2。
考点:考查了氧化还原反应、制备实验装置的作用的相关知识。


